题目内容
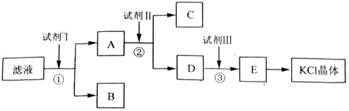
[2012·全国卷](12分)氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按如图所示步骤进行操作。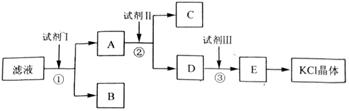
回答下列问题:
(1)起始滤液的pH__7(填“大于”、“小于”或“等于”),其原因是____________;
(2)试剂Ⅰ的化学式为______,①中发生反应的离子方程式为___________ ______;
(3)试剂Ⅱ的化学式为______,②中加入试剂Ⅱ的目的是____________ ________;
(4)试剂Ⅲ的名称是________,③中发生反应的离子方程式为_________ ____;
(5)某同学称取提纯的产品0.775 9 g,溶解后定容在100 mL容量瓶中,每次取25.00 mL溶液,用0.100 0 mol·L-1的硝酸银标准溶液滴定,三次滴定消耗标准溶液的平均体积为25.62 mL,该产品的纯度为_________________________________(列式并计算结果)。
(12分)(1)大于 弱酸强碱盐K2CO3发生水解使体系呈碱性
(2)BaCl2 Ba2++CO32-===BaCO3↓、Ba2++SO42-===BaSO4↓
(3)K2CO3 除去A中的Ba2+离子
(4)盐酸 CO32-+2H+===H2O+CO2↑
(5)×100%=98.40%
解析

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
[2012·全国卷] 能正确表示下列反应的离子方程式的是( )
| A.硫酸铝溶液中加入过量氨水:Al3++3OH-===Al(OH)3↓ |
| B.碳酸钠溶液中加入澄清石灰水:Ca(OH)2+CO32-===CaCO3↓+2OH- |
| C.冷的氢氧化钠溶液中通入氯气:Cl2+2OH-===ClO-+Cl-+H2O |
| D.稀硫酸中加入铁粉:2Fe+6H+===2Fe3++3H2↑ |