题目内容
19.2006年,发生在山西等地的瓦斯爆炸事故,造成多人伤亡,因此在矿井里,必须采取安全措施,如通风、严禁烟火等,而且要随时检查瓦斯的体积分数,当空气中混有5%---15%的甲烷时,遇到明火会发生爆炸,当爆炸最强烈时,甲烷的含量(体积分数)为( )(设空气中氧气含量为20%)| A. | 9.1% | B. | 10.5% | C. | 10% | D. | 5% |
分析 发生反应:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O,当甲烷与氧气体积之比为1:2时,发生最强烈爆炸,令甲烷的体积为1体积,计算氧气的体积,再根据空气中氧气的含量计算空气的体积,进而计算甲烷的体积分数.
解答 解:发生反应:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O可知,当甲烷与氧气体积之比为1:2时,发生最强烈爆炸,
设:混合气体的体积为100L,甲烷体积为VL,消耗O2的体积为2VL;空气体积(100-V)L;
则(100-V)×20%=2V;解得V=9.1L;
故此,发生爆炸最强烈时,甲烷在空气中所占的体积分数为:$\frac{9.1}{100}$×100%=9.1%,
故选A.
点评 本题考查混合物计算、根据方程式计算,难度不大,注意根据方程式确定甲烷与氧气的体积关系.

练习册系列答案
相关题目
7.在温度不变,恒荣的容器中进行反应2A?B+C,若反应物的浓度由0.1mol/L降到0.06mol/L需要20s,那么由0.06mol/L降到0.036mol/L需用时间可能为( )
| A. | 8s | B. | 10s | C. | 12s | D. | 14s |
14.我国科学家发现金丝桃素对高致病性禽流感病毒杀灭效果良好,某种金丝桃素的结构简式如图所示:
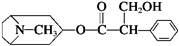
下列有关金丝桃素的说法:
①属于烃的衍生物,燃烧只产生CO2和H2O
②可以发生取代、加成、酯化、消去等反应
③分子式为C17H23O3N,苯环上的一氯取代物有3种
④1mol该物质最多能和6mol H2发生加成反应,
其中错误的是( )

下列有关金丝桃素的说法:
①属于烃的衍生物,燃烧只产生CO2和H2O
②可以发生取代、加成、酯化、消去等反应
③分子式为C17H23O3N,苯环上的一氯取代物有3种
④1mol该物质最多能和6mol H2发生加成反应,
其中错误的是( )
| A. | ①和④ | B. | ②和③ | C. | ①和③ | D. | ②和④ |
4.下列各组离子,在强碱性溶液中可以大量共存的是( )
| A. | K+ HCO3- NO3- ClO- | B. | Na+ SO32- NH4+ Ba2+ | ||
| C. | Ba2+ S2- Cl- SO42- | D. | AlO2- CO32- Cl- Na+ |
11.A、B、C、D、E、F是元素周期表中六种短周期元素,请根据表中信息回答下列问题
(1)元素B 的离子结构示意图 元素F的最高价氧化物的化学式为Cl2O7.
元素F的最高价氧化物的化学式为Cl2O7.
(2)元素A、D分别与元素C 形成原子个数比为1:2的化合物甲和1:1 的化合物乙,则甲属于非极性分子(填“极性”或“非极性”),化合物乙的电子式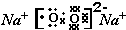 ,甲与乙反应的化学方程式为2CO2+2Na2O2=2Na2CO3+O2.
,甲与乙反应的化学方程式为2CO2+2Na2O2=2Na2CO3+O2.
(3)元素B、D组成化合物丙,其晶体类型为离子晶体,化合物丙的溶液呈碱性(填“酸性”“碱性”或“中性”).
(4)元素A与氢元素组成的最简单的化合物丁是一种优质燃料,燃烧热值高.
①实验测得,在常温常压下,1g化合物丁完全燃烧生成液态水,放出55.65kJ 热量.则表示化合物丁的燃烧热的热化学方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=890.4KJ/mol.
②某实验小组依据丁燃烧的反应原理,设计如图所示的电池装置.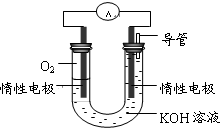
a.该电池正极的电极反应为O2+2H2O+4e-=4OH-.
b.工作一段时间后,测得溶液的pH减小,该电池总反应的离子方程式为CH4+2O2+2OH-=CO32-+3H2O.
(5)G也是短周期元素,其核外电子层数与最外层电子数相等,且与E处于元素周期表中对角线位置,它们的单质及其化合物的性质相似,写出G的氧化物与NaOH溶液反应的离子方程式:BeO+2OH-=BeO22-+H2O.若E的氯化物熔沸点较低、易升华,则E的氯化物是共价化合物(填“离子”或“共价”),试设计一个简单实验证明你的选择将其加热到熔融状态,做导电性实验,看其能否导电.
| 元素 | A | B | C | D | E | F |
性质或结构 信息 | 形成化合物种类最多的元素 | 最高正价是最低负价绝对值的3倍 | 族序数等于周期数的3倍 | 周期数是族序数的3倍 | 地壳中含量最高的金属元素 | 最高价氧化物对应水化物是最强的含氧酸 |
 元素F的最高价氧化物的化学式为Cl2O7.
元素F的最高价氧化物的化学式为Cl2O7.(2)元素A、D分别与元素C 形成原子个数比为1:2的化合物甲和1:1 的化合物乙,则甲属于非极性分子(填“极性”或“非极性”),化合物乙的电子式
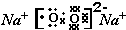 ,甲与乙反应的化学方程式为2CO2+2Na2O2=2Na2CO3+O2.
,甲与乙反应的化学方程式为2CO2+2Na2O2=2Na2CO3+O2.(3)元素B、D组成化合物丙,其晶体类型为离子晶体,化合物丙的溶液呈碱性(填“酸性”“碱性”或“中性”).
(4)元素A与氢元素组成的最简单的化合物丁是一种优质燃料,燃烧热值高.
①实验测得,在常温常压下,1g化合物丁完全燃烧生成液态水,放出55.65kJ 热量.则表示化合物丁的燃烧热的热化学方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=890.4KJ/mol.
②某实验小组依据丁燃烧的反应原理,设计如图所示的电池装置.

a.该电池正极的电极反应为O2+2H2O+4e-=4OH-.
b.工作一段时间后,测得溶液的pH减小,该电池总反应的离子方程式为CH4+2O2+2OH-=CO32-+3H2O.
(5)G也是短周期元素,其核外电子层数与最外层电子数相等,且与E处于元素周期表中对角线位置,它们的单质及其化合物的性质相似,写出G的氧化物与NaOH溶液反应的离子方程式:BeO+2OH-=BeO22-+H2O.若E的氯化物熔沸点较低、易升华,则E的氯化物是共价化合物(填“离子”或“共价”),试设计一个简单实验证明你的选择将其加热到熔融状态,做导电性实验,看其能否导电.
8.某结晶水合物的化学式为R•nH2O,其相对分子质量为M.25℃时,将a g该晶体溶于b g水中恰好可形成V mL饱和溶液.下列关系正确的是( )
| A. | 饱和溶液的物质的量浓度c=$\frac{1000a(M-18n)}{MV}$mol/L | |
| B. | 饱和溶液中溶质的质量分数w=$\frac{a(M-18n)}{M(a+b)}$% | |
| C. | 25℃时R的溶解度S=$\frac{100a(M-18n)}{18na+Mb}$g | |
| D. | 饱和溶液的密度ρ=$\frac{a(M-18n)}{a+b}$g/L |
 与
与 ⑥乙醇(CH3CH2OH)和甲醚(CH3OCH3);
⑥乙醇(CH3CH2OH)和甲醚(CH3OCH3); 和
和 ; ⑧
; ⑧ 和
和  .
.