题目内容
【题目】据《X-MOL》报道:RobertPipes等设计的添加PDS(![]() )的Li-CO2电池,正极物质转化原理如图所示。下列说法错误的是( )
)的Li-CO2电池,正极物质转化原理如图所示。下列说法错误的是( )
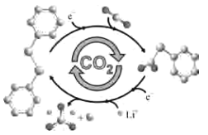
A.PDS起增强导电性作用
B.负极反应式为Li-e-=Li+
C.电池总反应为4Li+3CO2=2Li2CO3+C
D.正极上发生的反应之一为![]() +2CO2+2e-=2
+2CO2+2e-=2![]()
【答案】A
【解析】
A. 根据图中信息,PDS是非电解质,不导电,在流程中捕获CO2的作用,A错误;
B. 负极电极是金属Li,其电极反应式为Li-e-=Li+, B正确;
C. 由图中物质转化可知,PDS不消耗,因此电池总反应为4Li+3CO2=2Li2CO3+C,C正确;
D. 第一步PDS捕获CO2,发生的反应为![]() +2CO2+2e-=2
+2CO2+2e-=2![]() ,第二步发生的电极反应为6
,第二步发生的电极反应为6![]() +6e-=3
+6e-=3![]() + 2C + 4CO32-,D正确;
+ 2C + 4CO32-,D正确;
综上所述,答案为A。

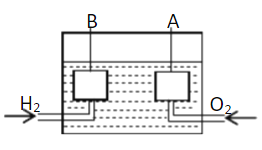
【题目】煤燃烧排放的烟气含有SO2和NOx,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。回答下列问题:
(1)在鼓泡反应器中通入含有SO2和NO的烟气,反应温度323K,NaClO2溶液浓度为5×10-3molL-1。反应一段时间后溶液中离子浓度的分析结果如下表。
离子 | SO | SO | NO | NO | Cl- |
c/(molL-1) | 8.35×10-4 | 6.87×10-6 | 1.5×10-4 | 1.2×10-5 | 3.4×10-3 |
①写出NaClO2溶液脱硝过程中主要反应的离子方程式___。增加压强,NO的转化率___(填“提高”、“不变”或“降低”)。
②随着吸收反应的进行,吸收剂溶液的pH逐渐___ (填“增大”、“不变”或“减小”)。
③由实验结果可知,脱硫反应速率脱硝反应速率___ (填“大于”或“小于”)。原因是除了SO2和NO在烟气中的初始浓度不同,还可能是___。
(2)在不同温度下,NaClO2溶液脱硫、脱硝的反应中SO2和NO的平衡分压pc如图所示。

①由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均___ (填“增大”、“不变”或“减小”)。
②反应ClO![]() +2SO
+2SO![]() =2SO
=2SO![]() +Cl-的平衡常数K表达式为___。
+Cl-的平衡常数K表达式为___。
(3)如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果。从化学平衡原理分析,Ca(ClO)2相比NaClO具有的优点是___。