题目内容
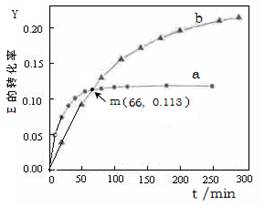
已知反应:2 E (l)  U (l) 。取等量的E,分别在20℃、50℃测得E的转化率随时间变化的关系曲线(Y-t)如右图所示。则下列说法正确的是( )
U (l) 。取等量的E,分别在20℃、50℃测得E的转化率随时间变化的关系曲线(Y-t)如右图所示。则下列说法正确的是( )

A.该反应的?H > 0
B.b代表50℃下E的Y-t曲线
C.m点(66,0.113)时有: ?n (E, 20℃) = ?n (E,50℃)
D.升高温度可以缩短达到平衡的时间,提高E的转化率
【答案】
C
【解析】
试题分析:由图可知,曲线a先达到平衡,因此a应为50℃下E的Y-t曲线。另外,从两条曲线的变化关系,可以得出:升高温度,E的转化率减少,故该反应为放热反应,?H<0。综上,答案为C。
考点:化学平衡
点评:本题结合坐标图考查了化学平衡移动,属于中等难度的题,也是高考中常见的考题。解题的关键在于读图坐标图,并结合相关知识点综合分析。对于坐标图的分析,可从“点、线、面”以及三者的结合入手。

练习册系列答案
 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
已知反应:2 E (l)  U (l) 。取等量的E,分别在20℃、50℃测得E的转化率随时间变化的关系曲线(Y-t)如右图所示。则下列说法正确的是( )
U (l) 。取等量的E,分别在20℃、50℃测得E的转化率随时间变化的关系曲线(Y-t)如右图所示。则下列说法正确的是( )
| A.该反应的?H > 0 |
| B.b代表50℃下E的Y-t曲线 |
| C.m点(66,0.113)时有: ?n (E, 20℃) = ?n (E,50℃) |
| D.升高温度可以缩短达到平衡的时间,提高E的转化率 |
 U (l) 。取等量的E,分别在20℃、50℃测得E的转化率随时间变化的关系曲线(Y-t)如图所示。则下列说法正确的是(
)
U (l) 。取等量的E,分别在20℃、50℃测得E的转化率随时间变化的关系曲线(Y-t)如图所示。则下列说法正确的是(
)
 U (l) 。取等量的E,分别在20℃、50℃测得E的转化率随时间变化的关系曲线(Y-t)如图所示。则下列说法正确的是(
)
U (l) 。取等量的E,分别在20℃、50℃测得E的转化率随时间变化的关系曲线(Y-t)如图所示。则下列说法正确的是(
)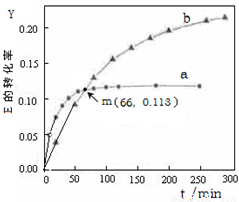
 U (l) 。取等量的E,分别在20℃、50℃测得E的转化率随时间变化的关系曲线(Y-t)如右图所示。
U (l) 。取等量的E,分别在20℃、50℃测得E的转化率随时间变化的关系曲线(Y-t)如右图所示。