题目内容
【题目】如图为乙酸丁酯制备的实验装置,下列说法正确的是
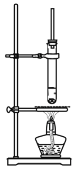
A.玻璃导管的主要作用是平衡试管内外压强
B.该装置适用于乙酸乙酯的制备
C.加入过量乙酸可以提高丁醇的转化率
D.分离提纯乙酸丁酯的方法是将混合物直接分液
【答案】C
【解析】
1-丁醇和乙酸在浓硫酸作用下,加热115~125℃,通过酯化反应制得乙酸丁酯,为可逆反应,反应中浓硫酸起到催化剂和吸水剂的作用,加入过量的乙酸,有利于平衡正向移动,有机物易挥发,长导管可起冷凝作用,以此解答该题。
A.玻璃导管的主要作用是冷凝回流,故A错误;
B.制备乙酸乙酯时,反应温度80℃左右,可以用水浴加热来控制温度,不能直接加热,故B错误;
C.制得乙酸丁酯,为可逆反应,加入过量的乙酸,有利于平衡正向移动,可以提高丁醇的转化率,故C正确;
D.提纯乙酸丁酯需使用碳酸钠溶液,吸收未反应的乙酸,溶解丁醇,降低乙酸丁酯的溶解度,故D错误;
答案选C。

 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案【题目】如表是元素周期表的一部分,根据表中给出的10种元素,按要求作答。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | N | O | F | Ne | ||||
3 | Na | Mg | Al | Si | S | Cl |
(1)金属性最强的元素是_______;
(2)F的原子结构示意图是________;
(3)地壳中含量最多的元素是_______;
(4)Ne原子的最外层电子数是_______;
(5)N与O原子半径较大的是_______;
(6)H2S与HCl热稳定性较弱的是______;
(7)Na2O与MgO难与水反应的是______;
(8)Mg(OH)2与Al(OH)3能与强碱反应的是______;
(9)用于制造光导纤维的物质是______(填“Si”或“SiO2”);
(10)次氯酸(HClO)具有杀菌漂白作用,其中Cl元素的化合价为____,HClO不稳定,易分解生成HCl和O2,写出其在光照条件下分解的化学方程式:____。