题目内容
B组命题正确,且能用A组命题加以正确解释的是( )
| A组 | B组 |
| Ⅰ.H-I键键能大于H-Cl键键能 | ①HI比HCl稳定 |
| Ⅱ.水分子之间可以形成氢键 | ②水分子很稳定 |
| Ⅲ.HI分子间作用力大于HCl分子间作用力 | ③HI沸点比HCl低 |
| Ⅳ.氨分子与水分子之间可以形成氢键 | ④氨极易溶于水 |
| A、Ⅰ① | B、Ⅱ② | C、Ⅲ③ | D、Ⅳ④ |
考点:化学键,含有氢键的物质
专题:化学键与晶体结构
分析:H-I>H-Cl的键长,键长越大,键能越小,分子越不稳定;HI的相对分子质量大于HCl的相对分子质量,二者结构相似,相对分子质量越大,沸点越高;氢键影响物质的物理性质不影响化学性质.
解答:
解:A.键能越大分子越稳定,H-I键键能小于H-Cl键键能,所以HCl比HI稳定,故A错误;
B.水分子稳定是因为水分子中H-O之间的化学键键能大,与氢键无关,故B错误;
D.HCl、HI结构相似,二者都是分子晶体,其相对分子质量越大,沸点越高,所以HI的沸点大于HCl,故C错误;
D.氨气分子和水分子之间能形成氢键,氢键的存在导致氨气溶解性增大,所以氨气极易溶于水,故D正确;
故选D.
B.水分子稳定是因为水分子中H-O之间的化学键键能大,与氢键无关,故B错误;
D.HCl、HI结构相似,二者都是分子晶体,其相对分子质量越大,沸点越高,所以HI的沸点大于HCl,故C错误;
D.氨气分子和水分子之间能形成氢键,氢键的存在导致氨气溶解性增大,所以氨气极易溶于水,故D正确;
故选D.
点评:本题考查化学键、氢键、分子间作用力等知识点,化学键影响物质的稳定性,氢键影响物质的熔沸点、溶解性等物理性质,注意化学键和氢键区别.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
已知下面三个数据:7.2×10-4 mol?L-1、4.6×10-4 mol?L-1、4.9×10-10 mol?L-1分别是下列有关的三种酸的电离常数,若已知下列反应可以发生:NaCN+HNO2═HCN+NaNO2 NaCN+HF═HCN+NaF NaNO2+HF═HNO2+NaF.由此可判断下列叙述不正确的是( )
| A、碱性强弱顺序:NaF<NaNO2<NaCN |
| B、K(HNO2)=4.9×10-10 mol?L-1 |
| C、一元弱酸的强弱顺序为HF>HNO2>HCN |
| D、K(HCN)<K(HNO2)<K(HF) |
1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学史上的重要里程碑之一.下列有关元素周期表的说法正确的是( )
| A、元素周期表有7个周期 |
| B、元素周期表有18个族 |
| C、第ⅠA族的元素全部是金属元素 |
| D、短周期是指第1、2、3、4周期 |
下列化学用语表示正确的是( )
| A、乙烯的结构简式:CH2CH2 | ||
B、S2-的结构示意图: | ||
C、中子数为20的氯原子:
| ||
D、羟基的电子式: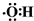 |

 (R、R′表示烃基)
(R、R′表示烃基)




 有氯原子的方法是
有氯原子的方法是 用选项中的电极、溶液和如图所示装置可组成原电池.下列现象或结论叙述正确的是( )
用选项中的电极、溶液和如图所示装置可组成原电池.下列现象或结论叙述正确的是( ) X、Y、Z、Q、R、W为周期表前四周期元素,原子序数依次递增,其中某些元素的相关信息如下表:
X、Y、Z、Q、R、W为周期表前四周期元素,原子序数依次递增,其中某些元素的相关信息如下表:
