题目内容
在汽车尾气处理装置中常发生如下反应:4CO+2NO2═4CO2+N2.下列对该反应的说法中正确的是( )
| A、该反应属于置换反应 | B、该反应中氧化剂是CO,还原剂是NO2 | C、该反应生成14gN2时,转移8mole- | D、该反应能减少汽车尾气对环境的污染 |
分析:4CO+2NO2═4CO2+N2中,C元素的化合价升高,N元素的化合价降低,结合氧化还原反应基本概念及转移电子解答.
解答:解:A.反应物中没有单质,不属于置换反应,故A错误;
B.C元素的化合价升高,CO为还原剂,N元素的化合价降低,氧化剂为NO2,故B错误;
C.该反应生成14gN2时,转移
×2×(4-0)=4mole-,故C错误;
D.CO、二氧化氮污染环境,而二氧化碳、氮气为无毒气体,则该反应能减少汽车尾气对环境的污染,故D正确;
故选D.
B.C元素的化合价升高,CO为还原剂,N元素的化合价降低,氧化剂为NO2,故B错误;
C.该反应生成14gN2时,转移
| 14g |
| 28g/mol |
D.CO、二氧化氮污染环境,而二氧化碳、氮气为无毒气体,则该反应能减少汽车尾气对环境的污染,故D正确;
故选D.
点评:本题考查氧化还原反应,为高频考点,把握氧化还原反应中元素的化合价变化为解答的关键,注意从化合价角度分析,侧重基本概念及转移电子和环境保护的考查,题目难度中等.

练习册系列答案
 期末集结号系列答案
期末集结号系列答案
相关题目
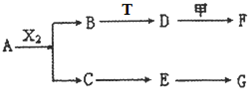 下列物质有如下转化关系(有的生成物未列出,反应条件均省略),其中:A在常温下是一种气体,能使湿润的红色石蕊试纸显蓝色,D为碱,G为酸,金属甲在G 的浓溶液中会钝化;F的溶液中只含一种溶质.
下列物质有如下转化关系(有的生成物未列出,反应条件均省略),其中:A在常温下是一种气体,能使湿润的红色石蕊试纸显蓝色,D为碱,G为酸,金属甲在G 的浓溶液中会钝化;F的溶液中只含一种溶质. N2 (g) +2CO2 ( g) 。
N2 (g) +2CO2 ( g) 。 