题目内容
下一代iPhone将在电池方面有所改进,该电池的一极为一种有机高分子游离基(用R表示)和石墨粉及粘结剂的复合材料,另一极是锂,分隔材料为某种聚烯烃,电解质为LiPF6溶解于某种有机碳酸酯溶剂中。该游离基(R)在空气中十分稳定,在充电时被氧化成阳离子(Rx+),电池充放电的方程式为:xLi+Rx+ xLi++R。下列有关说法正确的是
xLi++R。下列有关说法正确的是
| A.放电时,该电池将电能转化为化学能 | B.充电时,Rx+由阴极向阳极移动 |
| C.放电时,负极反应为xLi-xe-==xLi+ | D.充电时,阳极反应为R-xe-==Rx+ |
CD
解析试题分析:充电电池放电时为原电池,原电池是将化学能转化为电能的装置,故A选项错误;充电时为电解池,电解池中阳离子移向阴极,阴离子移向阳极,故B选项错误;由于xLi+Rx+== xLi++R中Li由0价升为+1价,失去电子,发生氧化反应,则负极反应式为xLi-xe-==xLi+,故C选项正确;由于xLi++R xLi+Rx+中R由0价升为+x价,失去电子,发生氧化反应,则阳极反应式为R-xe-==Rx+,故D选项正确。
xLi+Rx+中R由0价升为+x价,失去电子,发生氧化反应,则阳极反应式为R-xe-==Rx+,故D选项正确。
考点:考查新型充电电池,涉及原电池和电解池的判断、能量转化的形式、内电路中离子移动的方向、负极反应式、阳极反应式等。

用Pt做电极,电解含C(Cu2+): C(Na+): C(Cl-)=1:2:4的混合溶液,在任何情况下,阴、阳两极下不可能同时发生的反应是
| A.阴极:2H++2e-=H2↑阳极:4OH-- 4e-=2H2O+O2↑ |
| B.阴极:2H++2e-=H2↑阳极:2Cl--2e-=Cl2↑ |
| C.阴极:Cu2++2e-=Cu阳极:4OH-- 4e-=2H2O+O2↑ |
| D.阴极:Cu2++2e-=Cu阳极:2Cl--2e-=Cl2↑ |
用石墨作电极电解AgNO3溶液。通电一段时间后,欲使电解液恢复到起始状态,应向溶液中加入适量的( )
| A.AgNO3 | B.H2O | C.Ag2O | D.Ag(NH3)2OH |
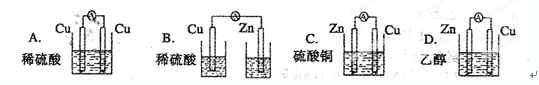
下列实验现象预测正确的是
| A.实验I:电流表A指针偏转,碳棒上有红色固体析出 |
| B.实验II:电流表A指针偏转,铁极上有无色气体产生 |
| C.实验III:碳棒上有无色气体产生,铁极上有黄绿色气体产生 |
| D.实验IV:粗铜溶解,精铜上有红色固体析出 |
“天宫一号”飞行器白天靠太阳能帆板产生电流向镍氢电池充电,夜间镍氢电池向飞行器供电。镍氢电池结构示意图如图。若电池总反应为:Ni(OH)2  NiOOH+1/2H2,充电时阴极反应为:H2O+e-=1/2H2+OH-。则下列说法正确的是
NiOOH+1/2H2,充电时阴极反应为:H2O+e-=1/2H2+OH-。则下列说法正确的是
| A.充电时a极为正极 |
| B.放电时NiOOH发生氧化反应 |
| C.充电时,K+向移a极,OH-移向b极 |
| D.放电时正极反应为:NiOOH + H2O +e-= Ni(OH)2 + OH- |
有关下列电化学装置的说法中正确的是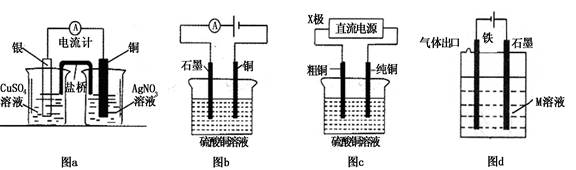
| A.图a是原电池装置,可以实现化学能转化为电能 |
| B.图b电解一段时间后,加入适量CuCO3固体,可以使硫酸铜溶液恢复到原浓度 |
| C.图c中的X极若为负极,则该装置可实现粗铜的精炼 |
| D.图d中若M是海水,该装置是通过“牺牲阳极的阴极保护法”使铁不被腐蚀 |
在化学能与电能的转化过程中,下列叙述正确的是 ( )
| A.电解饱和食盐水时,阳极得到Cl2 和NaOH(aq) |
| B.教材所示的铜-锌原电池在工作时,Zn2+ 向铜片附近迁移 |
| C.电镀时,电镀槽里的负极材料发生氧化反应 |
| D.原电池与电解池连接后,电子从原电池负极流向电解池阳极 |