题目内容
设NA表示阿伏加德罗常数,下列说法正确的是
- A.11.2L的CH4和NH3混合气体所含有的分子数目为0.5 NA
- B.1.5 mol 的NO2与足量H2O反应,转移的电子数为NA
- C.14g分子式为CnH2n的(n≥2)的链烃中含有的C=C的数目为
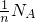
- D.6.2g氧化钠和7.8g过氧化钠混合物中所含有的离子数为0.7 NA
BC
分析:A.不一定是在标准状况下;
B.3NO2+H2O=2HNO3+NO反应中氮元素化合价既升高也降低,二氧化氮既作氧化剂又作还原剂,3mol的NO2中,2mol做还原剂,1mol做氧化剂;
C.烷烃(CnH2n+2)分子中不含共价键,烯烃(CnH2n)分子中含有1个双键,比烷烃少2个氢原子;
D.1mol氧化钠中含1mol钠离子和1mol氧离子;1mol过氧化钠中含2mol钠离子和1mol过氧根离子;
解答:A.因气体不一定是在标准状况下,Vm未知,无法计算,故A错误;
B.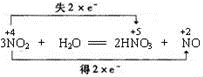 ,3mol的NO2反应,生成2mol硝酸转移2mol电子,所以1.5 mol 的NO2与足量H2O反应,转移的电子数为NA,故B正确;
,3mol的NO2反应,生成2mol硝酸转移2mol电子,所以1.5 mol 的NO2与足量H2O反应,转移的电子数为NA,故B正确;
C.与CnH2n碳原子个数相同的烷烃的分子式为CnH2n+2,CnH2n与CnH2n+2相比,减少的氢原子个数为2n+2-2n=2,少2个氢原子就多一个双键,所以CnH2n含有1个双键,14gCnH2n的物质的量为 =
=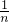 mol,含有的C=C的数目为为,
mol,含有的C=C的数目为为,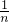 NA,故C正确;
NA,故C正确;
D.氧化钠的物质的量为 =0.1mol,1mol氧化钠中含1mol钠离子和1mol氧离子,所以6.2g氧化钠含有离子数为0.2 NA;过氧化钠的物质的量为
=0.1mol,1mol氧化钠中含1mol钠离子和1mol氧离子,所以6.2g氧化钠含有离子数为0.2 NA;过氧化钠的物质的量为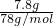 =0.1 mol,1mol过氧化钠中含2mol钠离子和1mol过氧根离子,所以7.8g过氧化钠含有离子数为0.3NA,该混合物中所含有的离子数为0.5NA,故D错误;
=0.1 mol,1mol过氧化钠中含2mol钠离子和1mol过氧根离子,所以7.8g过氧化钠含有离子数为0.3NA,该混合物中所含有的离子数为0.5NA,故D错误;
故选BC.
点评:本题考查了阿伏伽德罗常数的应用,主要考查物质的构成、发生的氧化还原反应、质量换算物质的量计算微粒数,题目难度中等.
分析:A.不一定是在标准状况下;
B.3NO2+H2O=2HNO3+NO反应中氮元素化合价既升高也降低,二氧化氮既作氧化剂又作还原剂,3mol的NO2中,2mol做还原剂,1mol做氧化剂;
C.烷烃(CnH2n+2)分子中不含共价键,烯烃(CnH2n)分子中含有1个双键,比烷烃少2个氢原子;
D.1mol氧化钠中含1mol钠离子和1mol氧离子;1mol过氧化钠中含2mol钠离子和1mol过氧根离子;
解答:A.因气体不一定是在标准状况下,Vm未知,无法计算,故A错误;
B.
 ,3mol的NO2反应,生成2mol硝酸转移2mol电子,所以1.5 mol 的NO2与足量H2O反应,转移的电子数为NA,故B正确;
,3mol的NO2反应,生成2mol硝酸转移2mol电子,所以1.5 mol 的NO2与足量H2O反应,转移的电子数为NA,故B正确;C.与CnH2n碳原子个数相同的烷烃的分子式为CnH2n+2,CnH2n与CnH2n+2相比,减少的氢原子个数为2n+2-2n=2,少2个氢原子就多一个双键,所以CnH2n含有1个双键,14gCnH2n的物质的量为
 =
=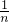 mol,含有的C=C的数目为为,
mol,含有的C=C的数目为为,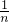 NA,故C正确;
NA,故C正确; D.氧化钠的物质的量为
 =0.1mol,1mol氧化钠中含1mol钠离子和1mol氧离子,所以6.2g氧化钠含有离子数为0.2 NA;过氧化钠的物质的量为
=0.1mol,1mol氧化钠中含1mol钠离子和1mol氧离子,所以6.2g氧化钠含有离子数为0.2 NA;过氧化钠的物质的量为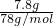 =0.1 mol,1mol过氧化钠中含2mol钠离子和1mol过氧根离子,所以7.8g过氧化钠含有离子数为0.3NA,该混合物中所含有的离子数为0.5NA,故D错误;
=0.1 mol,1mol过氧化钠中含2mol钠离子和1mol过氧根离子,所以7.8g过氧化钠含有离子数为0.3NA,该混合物中所含有的离子数为0.5NA,故D错误;故选BC.
点评:本题考查了阿伏伽德罗常数的应用,主要考查物质的构成、发生的氧化还原反应、质量换算物质的量计算微粒数,题目难度中等.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目