题目内容
【题目】苯甲醛在碱性条件下可发生反应: 2C6H5CHO + NaOH→C6H5CH2OH+C6H5COONa。相关物质的物理性质如下表:
苯甲醛 | 苯甲醇 | 苯甲酸 | 苯 | |||
溶 解 性 | 水中 | 微溶 | 微溶 | 温度 | 溶解度 | 不溶 |
17℃ | 0.21 g | |||||
25℃ | 0.34 g | |||||
100℃ | 5.9 g | |||||
有机溶剂中 | 易溶 | 易溶 | 易溶 | 易溶 | ||
密度(20℃)/g·cm-3 | 1.0 | 1.0 | 1.3 | 0.9 | ||
沸点/℃ | 178 | 205 | 249 | 80 | ||
熔点/℃ | 26 | -15 | 122 | 5.4 | ||
制备苯甲醇和苯甲酸的实验流程及涉及的主要实验装置(部分加热和固定装置已略)如下:
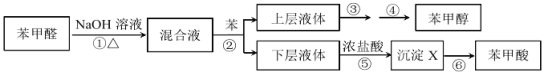
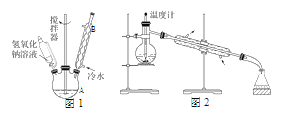
(1)第①步所用装置(如图 1),用搅拌器的目的是______________。仪器 B 的作用是_______________。
(2)第②步所用玻璃仪器有烧杯、_______________。
(3)第③步采用沸水浴加热蒸馏,收集到的馏分为_________;再进行第④步,操作如图 2 所示。图 2 中有一处明显错误,正确的应改为_________________________。
(4)第⑤步反应的离子方程式为________________________________________; 冷水洗涤沉淀 X 的优点是_________________________;检验沉淀 X 洗涤干净与否的操 作:______________。
(5)第⑥步经过滤、洗涤、干燥得苯甲酸产品,然后用电子天平准确称取 0.2440 g 苯甲酸样品于锥形瓶中,加 100 mL 蒸馏水溶解,再用 0.1000 mol·L-1 的标准 NaOH 溶液 进行滴定,经平行实验,测得消耗 NaOH 溶液的平均值为 19.20 mL,则苯甲酸样品的纯 度为_________ (质量百分数)。
【答案】加快NaOH与苯甲醛反应速率 冷凝回流 分液漏斗 苯 温度计的水银球放在蒸馏烧瓶的支管口处 C6H5COO-+H+→ C6H5COOH 取最后一次洗涤液少许于试管中,向试管中滴加硝酸酸化的硝酸银溶液,若无明显现象,则沉淀洗涤干净,若有白色沉淀生成,则沉淀没有洗涤干净 C6H5COOH+ NaOH=C6H5COONa+H2O 96%
【解析】
本题以苯甲醛为原料制备苯甲醇和苯甲酸的实验:结合题中已知信息和相关数据,苯甲醛与氢氧化钠溶液在加热条件下反应生成C6H5CH2OH和C6H5COONa。而C6H5CH2OH微溶于水,易溶于苯等有机溶剂,第②步操作加入苯,苯作萃取剂,苯的密度比水的密度小,上层液体是C6H5CH2OH的苯溶液,下层液体是C6H5COONa溶液,因为C6H5CH2OH与苯互溶,但是沸点不同,故采取蒸馏的方式把它们分离,C6H5COONa溶液中加入盐酸制取C6H5COOH。
(1)第①步搅拌器的目的是为了增加NaOH与苯甲醛的接触面积,加快NaOH与苯甲醛反应速率;仪器 B是球形冷凝管,起到冷凝回流的作用;
(2)第②步操作是萃取分液,用到的玻璃仪器有分液漏斗、烧杯;
(3)上层液体是C6H5CH2OH的苯溶液,第③步采用沸水浴加热蒸馏,水的沸点为100℃,由表中所给物质的沸点可知,苯的沸点80℃,C6H5CH2OH的沸点205℃,故收集到的馏分为苯;图2进行操作时,温度计的水银球插入液体中是错误的,蒸馏时,需要测量的蒸出的馏分蒸汽的温度,所以温度计的水银球应该放在蒸馏烧瓶的支管口处;
(4)第⑤步反应为强酸制弱酸,盐酸与C6H5COONa 反应生成C6H5COOH ,C6H5COO-+H+→ C6H5COOH;检验沉淀 X 洗涤干净,检验最后一次洗涤液中是否含有Cl-,操作如下:取最后一次洗涤液少许于试管中,向试管中滴加硝酸酸化的硝酸银溶液,若无明显现象,则沉淀洗涤干净,若有白色沉淀生成,则沉淀没有洗涤干净;
(5)C6H5COOH+ NaOH=C6H5COONa+H2O,n(C6H5COOH)=n(NaOH)= 0.1000×19.20×10-3=1.920×10-3 mol,则苯甲酸样品的纯度为![]() ×100%=96% 。
×100%=96% 。

 优学名师名题系列答案
优学名师名题系列答案【题目】如图是利用废铜屑(含杂质铁)制备胆矾(硫酸铜晶体)的流程。
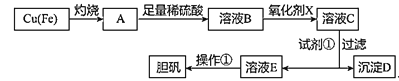
溶液中被沉淀离子 | Fe3+ | Fe2+ | Cu2+ |
完全生成氢氧化物沉淀时,溶液的pH | ≥3.7 | ≥6.4 | ≥4.4 |
请回答:
(1)溶液B中含有的阳离子有__(填离子符号)。
(2)下列物质中最适宜做氧化剂X的是__(填字母)。
A.NaClO B.H2O2 C.KMnO4
写出加入氧化剂X时,发生反应的离子方程式___。
(3)加入试剂①是为了调节pH,试剂①可以选择__(填化学式)。
已知:残留在溶液中的离子浓度小于1×10-5mol/L时,沉淀就达完全。则Fe(OH)3的溶度积常数Ksp=___。
(4)操作①的步骤:___、___、过滤、洗涤、干燥。
(5)沉淀D加入盐酸可以得到FeCl3,关于FeCl3溶液的性质中说法不正确的是__。
A.将FeCl3饱和溶液逐滴加入沸水中,并继续加热得到红褐色液体,该液体能产生丁达尔效应
B.将FeCl3溶液滴加到淀粉-KI溶液中,溶液显蓝色
C.将FeCl3溶液加热蒸干并灼烧,得到FeCl3固体
D.向FeCl3溶液中滴加KSCN溶液,溶液中出现红色沉淀
【题目】化学是一门以实验为基础的科学。
(1)用下列实验装置完成对应的实验(部分仪器略去),能达到实验目的的是_____(填字母)。
A | B | C | D |
|
|
|
|
干燥氯气 | 吸收NH3 | 石油的分馏 | 制取乙酸乙酯 |
(2)为除去粗盐中的MgCl2、CaCl2、Na2SO4以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
称取粗盐![]() 滤液
滤液![]() 精盐
精盐
①第Ⅰ步操作的名称是______。
②若第Ⅱ、Ⅳ步顺序颠倒,是否会对实验结果产生影响?_____(填“有影响”或“无影响”)。
③第Ⅴ步操作所需玻璃仪器的名称是________。





