题目内容
17.在下列条件下,两种气体的分子数一定相等的是( )| A. | 同温度、同体积的N2和O2 | B. | 同压强、同体积的H2和CH4 | ||
| C. | 同质量、不同密度的N2和CO | D. | 同体积、同密度的CO2和N2 |
分析 A.由于气体的压强不一定相同,所以分子数不一定相等;
B.温度不同,则气体分子之间的距离可能不同,其分子数不一定相等;
C.CO、N2摩尔质量相同,则等质量的两种物质的物质的量相同;
D.同体积、同密度的二氧化碳和氮气其质量相同,因为摩尔质量不同,二者物质的量不相同.
解答 解:A.影响气体体积的外因是温度和压强,由于气体的压强不一定相同,所以分子数不一定相等,故A错误;
B.温度不同,则气体分子之间的距离可能不同,因此其分子数不一定相等,故B错误;
C.CO、N2摩尔质量相同,则等质量的两种物质的物质的量相同,因此分子数一定相同,故C正确;
D.同体积、同密度的二氧化碳和氮气其质量相同,因为摩尔质量不同,二者物质的量不相同,所以其分子数一定不同,故D错误,
故选:C.
点评 本题考查阿伏加德罗定律的应用,难度不大,注意理解气体摩尔体积的影响因素.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
7.某研究性学习小组利用下列有关装置对SO2的性质及空气中SO2的含量进行探究(装置的气密性已检查):
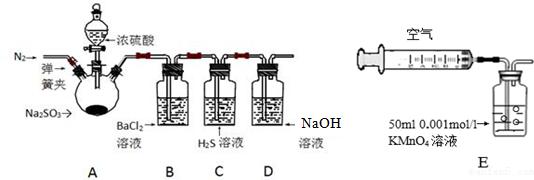
(1)装置A中反应的化学方程式是Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O.
(2)滴加浓硫酸之前,打开弹簧夹,通入一段时间N2,再关闭弹簧夹.此操作的目的是排除装置中氧气对实验的干扰.
(3)实验过程装置B中没有明显变化.实验结束取下装置B,从中分别取少量溶液于两支洁净试管中.向第1支试管中滴加适量氨水出现白色沉淀BaSO3(填化学式);向第2支试管中滴加适量新制氯水,仍然出现白色沉淀,该反应的离子方程式是Ba2++SO2+Cl2+2H2O=BaSO4↓+4H++2Cl-.
(4)装置C中的溶液中出现淡黄色浑浊,该实验证明SO2具有氧化 性.
(5)装置D的作用是吸收SO2尾气,防止污染空气.
(6)实验后,测定装置D中溶液呈碱性.溶液为什么呈碱性呢?大家有两种不同的假设:①是生成的Na2SO3水解;②是氢氧化钠剩余.请设计实验方案证明哪种假设成立.可任选下列试剂进行实验:Na2SO3溶液、酚酞溶液、氯水、BaCl2溶液、稀硫酸
(7)另一小组利用装置E进行实验:SO2性质实验之后,用注射器对实验室内空气进行取样.并向装置E中共注入V mL(已折算为标况下体积)的空气,当溶液刚好褪色时,停止实验.请计算该空气中SO2的体积分数(用含V的代数式表示)$\frac{2.8}{V}$.

(1)装置A中反应的化学方程式是Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O.
(2)滴加浓硫酸之前,打开弹簧夹,通入一段时间N2,再关闭弹簧夹.此操作的目的是排除装置中氧气对实验的干扰.
(3)实验过程装置B中没有明显变化.实验结束取下装置B,从中分别取少量溶液于两支洁净试管中.向第1支试管中滴加适量氨水出现白色沉淀BaSO3(填化学式);向第2支试管中滴加适量新制氯水,仍然出现白色沉淀,该反应的离子方程式是Ba2++SO2+Cl2+2H2O=BaSO4↓+4H++2Cl-.
(4)装置C中的溶液中出现淡黄色浑浊,该实验证明SO2具有氧化 性.
(5)装置D的作用是吸收SO2尾气,防止污染空气.
(6)实验后,测定装置D中溶液呈碱性.溶液为什么呈碱性呢?大家有两种不同的假设:①是生成的Na2SO3水解;②是氢氧化钠剩余.请设计实验方案证明哪种假设成立.可任选下列试剂进行实验:Na2SO3溶液、酚酞溶液、氯水、BaCl2溶液、稀硫酸
| 实验步骤 | 实验操作 | 预期现象与结论 |
| 1 | 取少量溶液于试管中,滴入几滴酚酞 | 溶液变红 |
| 2 |
8.在一种酸性溶液中,可能存在NO3-、I-、Cl-、Fe3+中的一种或几种离子,向该溶液中加入溴水,溴单质被还原,则以下推测中不正确的是( )
| A. | 一定有I- | B. | 可能含Fe3+ | C. | 可能有Cl- | D. | 不含NO3- |
5.下列哪种物质所含原子数与0.3molH2O2所含原子数相等( )
| A. | 0.6molCaO | B. | 0.2molH2SO4 | C. | 0.15molH3PO4 | D. | 0.4molMgCl2 |
9.在1.00L 1mol/L氢氧化钠溶液中通入16.8L标准状况下的CO2气体,所得的溶液中含有的溶质是( )
| A. | Na2CO3 | B. | NaHCO3 | ||
| C. | Na2CO3和NaHCO3 | D. | NaOH、Na2CO3和NaHCO3 |
6.下列有关实验操作与结论都正确的是( )
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某钠盐中加入稀盐酸,产生能使澄清石灰水变浑浊的气体 | 说明该盐一定是碳酸盐 |
| B | 向某无色溶液中滴加BaCl2溶液,再滴加过量的稀HNO3,产生白色沉淀 | 该无色溶液中一定有SO42- |
| C | 向某无色溶液中滴加NaOH溶液,加热后,产生是湿润的红色石蕊试纸变蓝的气体 | 说明溶液液中含有NH4+ |
| D | 某无色气体通过灼热的CuO,CuO变为红色 | 该气体一定为氢气 |
| A. | A | B. | B | C. | C | D. | D |
 在一恒温恒容密闭容器中,某化学反应2A(g)?B(g)+C(g)在三种不同条件下进行,其中实验Ⅰ、Ⅱ在800℃,实验Ⅲ在820℃,B、C的起始浓度都为0,反应物A的浓度(mol•L-1)随时间(min)变化如图所示.
在一恒温恒容密闭容器中,某化学反应2A(g)?B(g)+C(g)在三种不同条件下进行,其中实验Ⅰ、Ⅱ在800℃,实验Ⅲ在820℃,B、C的起始浓度都为0,反应物A的浓度(mol•L-1)随时间(min)变化如图所示.