题目内容
17.用惰性电极插入KOH溶液中,在两极分别通入CH3OH和O2,有关此电池判断正确的是( )| A. | 正极反应式:2CH3OH+2H2O-12e-═2CO2↑+12H+ | |
| B. | 放电一段时间后,负极的PH值升高 | |
| C. | 放电一段时间,阳离子向负极移动,阴离子向正极移动 | |
| D. | 该电池在工作时,每消耗32gCH3OH,外电路中通过6mole- |
分析 燃料碱性电池中通入甲醇的一极为原电池的负极,发生氧化反应,CH4O-6e-+8OH-=CO32-+6H2O,通入氧气的一极为原电池的正极,发生还原反应,电极反应式为2H2O+O2+4e-=4OH-,放电时,电解质溶液中阳离子向正极移动、阴离子向负极移动,结合甲醇和转移电子正极关系式分析解答.
解答 解:A.该电解质溶液是碱性溶液,正极上氧气得电子发生还原反应,负极上甲醇失电子和氢氧根离子反应生成碳酸根离子,负极、正极反应式分别为CH4O-6e-+8OH-=CO32-+6H2O、2H2O+O2+4e-=4OH-,故A错误;
B.负极反应式为CH4O-6e-+8OH-=CO32-+6H2O,氢氧根离子参加反应导致溶液碱性减小,pH降低,故B错误;
C.放电时,阳离子向正极移动,阴离子向负极移动,故C错误;
D.n(CH3OH)=$\frac{32g}{32g/mol}$=1mol,根据CH4O-6e-+8OH-=CO32-+6H2O知,每消耗32gCH3OH,外电路中通过6mole-,故D正确;
故选D.
点评 本题考查化学电源新型电池,为高频考点,所有燃料电池中负极上都是燃料失电子、正极上都是氧化剂得电子,难点是电极反应式的书写,要结合电解质溶液酸碱性书写,为学习难点.

练习册系列答案
相关题目
12.在下列各溶液中,离子一定能大量共存的是( )
| A. | 室温下,pH=1的溶液中:Na+、Fe3+、NO3-、SO42- | |
| B. | 碱性溶液中:K+、Mg2+、S2-、ClO- | |
| C. | 加入铝粉有气泡产生的溶液中:Na+、NH4+、Fe2+、NO3- | |
| D. | 在AlCl3溶液中:K+、Na+、SiO32-、SO42- |
2.电动自行车由于灵活、快捷、方便,已成为上班族的主要代步工具,其电源常采用铅蓄电池,反应原理为PbO2+Pb+2H2SO4$?_{充电}^{放电}$2PbSO4+2H2O,下列叙述正确的是( )
| A. | 电池放电时,PbO2是电池的正极,被氧化 | |
| B. | 电池放电时,SO42-只在负极发生反应 | |
| C. | 电池充电时,溶液的pH不断增大 | |
| D. | 电池充电时,阳极反应式为PbSO4+2H2O-2e-═PbO2+SO42-+4H+ |
9.下列说法正确的是( )
| A. | 煤的主要组成为苯以及苯的同系物 | |
| B. | “可燃冰”为水可能变成油提供了有力的证据 | |
| C. | 油脂、淀粉、纤维素、蛋白质都是高分子化合物 | |
| D. | 石油的裂解是使石油分馏产物中的长链烃断裂成乙烯、丙烯等气态短链烃 |
6.已知维生素A的结构简式如图.关于它的叙述正确的是( )
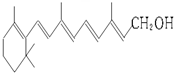

| A. | 维生素A的分子式为C20H30O | |
| B. | 1 mol维生素A最多可与 7 mol H2发生加成反应 | |
| C. | 维生素A分子中含有羟基、碳碳双键和苯环等官能团 | |
| D. | 维生素A是一种易溶于水的醇 |
 某同学应用右图所示的方法研究物质的性质,其中气体A的主要成分是氯气,杂质是空气和水蒸气.回答下列问题:
某同学应用右图所示的方法研究物质的性质,其中气体A的主要成分是氯气,杂质是空气和水蒸气.回答下列问题: .
. 三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在半导体加工、太阳能电池制造和液晶显示器制造中得到广泛应用.它可在铜的催化作用下由F2和过量的NH3反应得到,该反应另一种产物为盐.
三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在半导体加工、太阳能电池制造和液晶显示器制造中得到广泛应用.它可在铜的催化作用下由F2和过量的NH3反应得到,该反应另一种产物为盐. .
. )对花香和果香的香韵具有提升作用,故常用于化妆品工业和食品工业.它有很多同分异构体,其中含有酯基和一取代苯结构的同分异构体有五个,请写出其结构简式:
)对花香和果香的香韵具有提升作用,故常用于化妆品工业和食品工业.它有很多同分异构体,其中含有酯基和一取代苯结构的同分异构体有五个,请写出其结构简式: 、
、 、
、 、
、 、
、 .
.