题目内容
下列说法正确的是
| A.L层上的电子数为奇数的原子一定是主族元素的原子 |
| B.元素周期表共有18列,第8列属于第ⅧB族、第17列属于第VIIA族 |
| C.化学键的形成一定伴随着电子的转移和能量变化 |
| D.元素周期表中,位于金属和非金属交界线附近的元素属于过渡元素 |
A
解析试题分析:A、L层上的电子数为奇数的原子位于第二周期,一定是主族元素的原子,正确;B、元素周期表共有18列,第8列属于第Ⅷ族、第17列属于第VIIA族,错误;C、化学键的形成不一定伴随着电子的转移,如蒸发氯化钠溶液的氯化钠晶体,形成了离子键但没有电子转移,错误;D、元素周期表中,位于第ⅢB族到ⅡB族的10个纵行的元素属于过渡元素,错误。
考点:考查原子结构、元素周期律和元素周期表。

练习册系列答案
相关题目
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y原子的最外层电子数是其电子层数的3倍。下列说法正确的是( )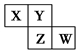
| A.元素W的最高价氧化物对应水化物的酸性最强 |
| B.单核阴离子半径的大小顺序为:r(W)>r(Z) >r(Y) |
| C.元素Y和元素Z的氢化物中均只存在极性共价键 |
| D.元素Y和元素Z的最高正化合价相同 |
W、X、Y、Z是短周期元素,其部分性质如下表
| W | 单质是淡黄色固体 |
| X | 在地壳中的含量居第二位 |
| Y | 原子最外层电子数是电子总数的2/3 |
| Z | 第三周期原子半径最小的金属 |
下列说法正确的是
A.Z的氧化物属于碱性氧化物
B.最高价氧化物对应水化物的酸性:Y>X
C.离子半径:Z>W
D.气态氢化物的热稳定性:X>W
月球含有丰富的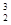 He。下列关于
He。下列关于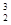 He的说法不正确的是 ( )
He的说法不正确的是 ( )
A.核外电子排布为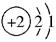 |
| B.原子核内有1个中子 |
C.与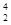 He互为同位素 He互为同位素 |
D.比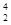 He具有相同的质子数 He具有相同的质子数 |
下列微粒半径大小比较错误的是( )。
| A.K>Na>Li | B.Na+>Mg2+>Al3+ |
| C.Mg2+>Na+>F- | D.Cl->F->F |
首次将量子化概念应用到原子结构,并解释了原子的稳定性的科学家是( )。
| A.道尔顿 | B.爱因斯坦 | C.玻尔 | D.普朗克 |
关于npx和npy的叙述中,正确的是( )。
| A.它们是同一条轨道 |
| B.二者能量相同 |
| C.二者电子云在空间的伸展方向相同 |
| D.电子云形状不同 |
1913年,丹麦科学家玻尔第一次认识到氢原子光谱是氢原子的电子跃迁产生的。玻尔的原子结构理论一个很大的成就是( )。
| A.证明了原子核外电子在圆形轨道上运动 |
| B.提出了原子核是可以进一步细分的 |
| C.解决了氢原子光谱和原子能级之间的关系 |
| D.应用了量子力学理论中的概念和方法 |
X、Y、Z是三种短周期元素,其中X、Y位于同一主族,Y、Z处于同一周期。X原子的最外层电子数是其电子层数的3倍。Z原子的核外电子数比Y原子少1。下列说法正确的是( )。
| A.元素非金属性由弱到强的顺序为Z<Y<X |
| B.Y元素最高价氧化物对应水化物的化学式可表示为H3YO4 |
| C.三种元素的气态氢化物中,Z的气态氢化物最稳定 |
| D.原子半径由大到小的顺序为Z<Y<X |