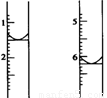题目内容
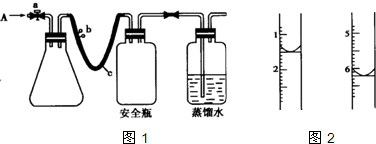
向Na2S2O3和Na2S的混合溶液中缓慢滴入足量的稀H2SO4,完全反应后,得到3.20g沉淀和336mL气体(标准状况),溶液总体积为100mL,溶液中H2S的浓度为0.100mol·L-1.
(1)写出各反应的化学方程式.
(2)336mL气体是什么气体,为什么?
(3)求原混合溶液中Na2S2O3和Na2S的物质的量.
答案:
解析:
解析:
|
(1)Na2S2O3+H2SO4=Na2SO4+H2O+SO2↑+S↓ Na2S+H2SO4=Na2SO4+H2S↑ 2H2S+SO2=H2O+3S (2)H2S气体 溶液中有H2S,SO2与H2S不能共存. (3)解:溶液中H2S的物质的量:0.100mol·L-1×0.100mol·L=0.010mol H2S气体的物质的量:336mL/22400mL·mol-1=0.0150mol 设:Na2S2O3物质的量为x 关系式:Na2S2O3~2Na2S~4S 1mol 2mol 4mol x 2x x=0.0250mol 2x=0.0500mol 所以,原混合液中n(Na2S2O3)=0.0250mol n(Na2S)=(0.0500+0.0100+0.0150)mol=0.0750mol |

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
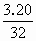 mol
mol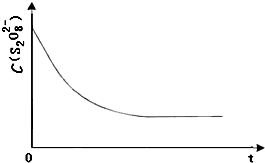 碘在科研与生活中有重要应用.某兴趣小组用0.50mol?L-1KI、0.2%淀粉溶液、0.20mol?L-1K2S2O8、0.10mol?L-1Na2S2O3等试剂,探究反应条件对化学反应速率的影响.
碘在科研与生活中有重要应用.某兴趣小组用0.50mol?L-1KI、0.2%淀粉溶液、0.20mol?L-1K2S2O8、0.10mol?L-1Na2S2O3等试剂,探究反应条件对化学反应速率的影响.