��Ŀ����
16��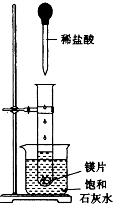 ��ͼ��ʾ�����Թܷ���ʢ��25��ı���ʯ��ˮ���ձ��У��Թ��п�ʼ���뼸С��þƬ�����õιܵ���5mL�������Թ��У��Իش����лش�
��ͼ��ʾ�����Թܷ���ʢ��25��ı���ʯ��ˮ���ձ��У��Թ��п�ʼ���뼸С��þƬ�����õιܵ���5mL�������Թ��У��Իش����лش���1��ʵ���й۲쵽��������ABD����ѡ����ţ�3�֣�
A���Թ���þƬ���ܽ�
B���Թ��в�����ɫ����
C���ձ���ڱ���
D���ձ��ײ�����������ɫ����
��2���Թ��з����ķ�Ӧ����������ԭ��Ӧ��ѡ�������ԭ��Ӧ����������ԭ��Ӧ������
��3��д���йط�Ӧ�����ӷ���ʽMg+2H+=Mg2++H2����
��4����ʵ����֪��MgCl2��Һ��H2��������С�ڣ�����ڡ���С�ڡ������ڡ���þƬ���������������
���� ��1��Mgλ����֮ǰ���ܺ�ϡ���ᷴӦ�����������÷�Ӧ�Ƿ��ȷ�Ӧ���ų�������ʹ�ձ�����Һ�¶����ߣ����������ܽ�������¶����߶���С��
��2���е���ת�ƵĻ�ѧ��Ӧ��������ԭ��Ӧ��
��3�����ʡ����塢������д��ѧʽ��������ǿ�����д���ӣ�
��4�����ȷ�Ӧ�з�Ӧ��������������������������
��� �⣺��1��Mgλ����֮ǰ���ܺ�ϡ���ᷴӦ�����������÷�Ӧ�Ƿ��ȷ�Ӧ���ų�������ʹ�ձ�����Һ�¶����ߣ����������ܽ�������¶����߶���С��
A��þ��ϡ���ᷴӦ�����Ȼ�þ�������������Թ���þƬ���ܽ⣬����ȷ��
B�����������������Թ��в�����ɫ���ݣ�����ȷ��
C����������ķ�Ӧ�Ƿ��ȷ�Ӧ�������ձ���ڱ��ȣ��ʴ���
D�����������ܽ�������¶����߶���С�������¶ȣ��������Ʊ�����Һ��Ϊ��������Һ�������ձ��ײ�����������ɫ���壬����ȷ��
��ѡABD��
��2�����������ӷ�ӦΪMg+2H+=Mg2++H2�����÷�Ӧ���е���ת�ƣ���������������ԭ��Ӧ���ʴ�Ϊ��������ԭ��Ӧ��
��3�����ʡ����塢������д��ѧʽ��������ǿ�����д���ӣ����ӷ���ʽΪMg+2H+=Mg2++H2�����ʴ�Ϊ��Mg+2H+=Mg2++H2����
��4�����ȷ�Ӧ�з�Ӧ���������������������������÷�Ӧ�Ƿ��ȷ�Ӧ������MgCl2��Һ��H2��������С��þƬ����������������ʴ�Ϊ��С�ڣ�
���� ������þ����������Ϊ���忼�������غ㡢������ԭ��Ӧ�����ӷ���ʽ����д��֪ʶ�㣬��ȷʵ��ԭ���ǽⱾ��ؼ���ע���������������Һ�仯����Ŀ�ѶȲ���

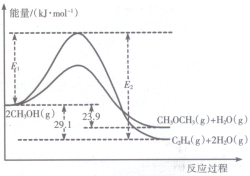 ������Ҫ���л�����ԭ�ϣ�һ�������£��״���ͬʱ��������������Ӧ��
������Ҫ���л�����ԭ�ϣ�һ�������£��״���ͬʱ��������������Ӧ��i.2CH3OH��g��?CH3OCH3��g��+H2O��g��
ii.2CH3OH��g��?C2H4��g��+2H2O��g��
I��������Ӧ�����������仯��ͼ��ʾ��
��1����ij�ܱ������У�����һ����CH3OH��g����������������Ӧ����Ӧi���i����ii���������ʽϴ���ԭ��Ϊ�÷�Ӧ�Ļ�ܽ�С�����������м��������ʹii�ķ�Ӧ����������E1��E2-E1�ı仯�ǣ�E1��С��E2-E1���䣨���������С�����䡱����
��2����֪��CH3CH2OH��g��=CH3OCH3��g����H=+50.7kJ��mol-1������ϩ����ֱ��ˮ�Ϸ�ӦC2H4��g��+H2O��g��=C2H5OH��g���ġ�H=-45.5kJ•mol-1��
��ij�о�С��ͨ�����Ʒ�Ӧ�������������ݻ���Ϊ2L���ܱ�������ֻ������Ӧi����ʼ��Ӧ�¶Ⱦ�ΪT�棬��ʼͶ�����±���ʾ��
| ��ʼͶ��/mol ��� | CH3OH��g�� | CH3OCH3��g�� | H2O��g�� |
| ��������1 | 2 | 0 | 0 |
| ��������2 | 0 | 2 | 2 |
| ��������3 | 2 | 0 | 0 |
��4��������l��ƽ��ʱCH3OH��g�� ��ת����Ϊ80%������¶��·�Ӧi��ƽ�ⳣ��K=4��
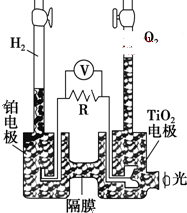 TiO2�ڹ������¿�ʹˮ�ֽ⣺2H2O$\frac{\underline{\;TiO_{2}\;}}{��}$2H2��+O2�����ù�������ֲ��Ĺ�����ã���ͼ�ǹ�������TiO2�ֽ�ˮ��װ��ʾ��ͼ������������ȷ���ǣ�������
TiO2�ڹ������¿�ʹˮ�ֽ⣺2H2O$\frac{\underline{\;TiO_{2}\;}}{��}$2H2��+O2�����ù�������ֲ��Ĺ�����ã���ͼ�ǹ�������TiO2�ֽ�ˮ��װ��ʾ��ͼ������������ȷ���ǣ�������| A�� | TiO2�缫�Ϸ����ķ�ӦΪ��2H++2e-�TH2�� | |
| B�� | ��װ�ù���ʱ��TiO2�缫������Һ��pH��� | |
| C�� | ��װ�ù���ʱ��������TiO2�缫��R���缫 | |
| D�� | ��װ�ÿ��Խ�����ת��Ϊ���ܣ�ͬʱҲ�ܽ���ת��Ϊ��ѧ�� |
 һ���¶��£�����̼����MCO3��M��Mg2+��Ca2+��Mn2+���ij����ܽ�ƽ��������ͼ��ʾ����֪��pX=-lgc��X��������˵����ȷ���ǣ�������
һ���¶��£�����̼����MCO3��M��Mg2+��Ca2+��Mn2+���ij����ܽ�ƽ��������ͼ��ʾ����֪��pX=-lgc��X��������˵����ȷ���ǣ�������| A�� | �ڸ��¶��£�MgCO3��MnCO3 ���ܽ���������� | |
| B�� | d��ɱ�ʾMnCO3�Ĺ�������Һ����c��Mn2+����c��CO32-�� | |
| C�� | b��ɱ�ʾCaCO3�ı�����Һ����c��Ca2+����c��CO32-�� | |
| D�� | c��ɱ�ʾMgCO3 �IJ�������Һ����c��Mg2+����c��CO32-�� |
| A�� | H2��D2 | B�� | T2O��H2O | ||
| C�� | ${\;}_{19}^{40}$K��${\;}_{19}^{39}$K | D�� | ���ʯ��ʯī |
| A�� | 18ml | B�� | ����18ml | C�� | С��18ml | D�� | ���ж� |
| A�� | �ƺ���ˮ��Ӧ��Na+2H2O�TNa++OH-+H2�� | |
| B�� | �����������������ƣ�Al+2OH-�TAlO2-+H2�� | |
| C�� | ����������������2Al+6H+�T2Al3++3H2�� | |
| D�� | ����ϡ���ᷴӦ��Fe+2H+�TFe3++H2�� |
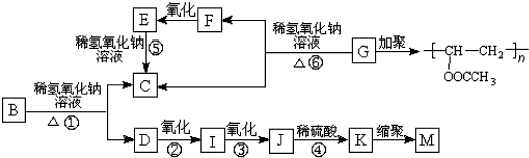
 ��
��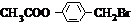 +3NaOH$��_{��}^{ˮ}$CH3COONa+
+3NaOH$��_{��}^{ˮ}$CH3COONa+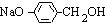 +NaBr+H2O��
+NaBr+H2O��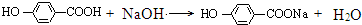 ��
��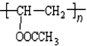 ������������Һ�м��ȣ�
������������Һ�м��ȣ�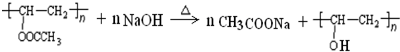 ��
��