题目内容
高锰酸钾和盐酸溶液可以发生以下反应:
2KMn04+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
(1)用双线桥标出该反应中电子转移的方向和数目.
(2)该反应的氧化产物是______.
(3)若消耗0.2mol氧化剂,则被氧化的还原剂的物质的量是______mol.
解:根据反应2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O中元素化合价的变化,可得该反应电子转移的方向和数目如下所示: ,故答案为:
,故答案为: ;
;
(2)化合价升高的元素是浓盐酸中的氯元素,所得到的氧化产物是氯气,故答案为:Cl2;
(3)高锰酸钾是氧化剂,还原剂是浓盐酸,2mol高锰酸钾氧化剂消耗的16mol浓盐酸中,只有10mol浓盐酸做还原剂,所以氧化剂和被氧化的还原剂的量之间的关系为:2KMn04~10HCl,若消耗0.2mol氧化剂,则被氧化的还原剂的物质的量1mol,故答案为:1.
分析:(1)氧化还原反应中失电子的元素化合价升高,得电子的元素化合价降低,化合价降低数目=化合价升高数目=转移的电子数目;
(2)化合价升高元素所在的生成物是氧化产物;
(3)化合价降低元素所在的反应物是氧化剂,化合价升高元素所在的反应物是还原剂,根据化学方程式计算氧化剂和还原剂之间量的关系.
点评:本题考查氧化还原反应的特征和实质以及根据化学方程式的计算知识,是对教材知识的考查,难度不大.
 ,故答案为:
,故答案为: ;
;(2)化合价升高的元素是浓盐酸中的氯元素,所得到的氧化产物是氯气,故答案为:Cl2;
(3)高锰酸钾是氧化剂,还原剂是浓盐酸,2mol高锰酸钾氧化剂消耗的16mol浓盐酸中,只有10mol浓盐酸做还原剂,所以氧化剂和被氧化的还原剂的量之间的关系为:2KMn04~10HCl,若消耗0.2mol氧化剂,则被氧化的还原剂的物质的量1mol,故答案为:1.
分析:(1)氧化还原反应中失电子的元素化合价升高,得电子的元素化合价降低,化合价降低数目=化合价升高数目=转移的电子数目;
(2)化合价升高元素所在的生成物是氧化产物;
(3)化合价降低元素所在的反应物是氧化剂,化合价升高元素所在的反应物是还原剂,根据化学方程式计算氧化剂和还原剂之间量的关系.
点评:本题考查氧化还原反应的特征和实质以及根据化学方程式的计算知识,是对教材知识的考查,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列实验操作中不正确的是( )(填序号)
| A、用托盘天平称取11.70g食盐 | B、利用任何强酸和强碱溶液相互反应均可测得中和热为57.3kJ/mol | C、用量筒量取12.36mL盐酸 | D、用酚酞作指示剂进行中和滴定时,当溶液由无色变为红色时立即停止滴定 | E、用酸式滴定管盛装高锰酸钾溶液进行相关滴定 |
某同学用如图所示的装置来制取和探究气体(H2、O2、Cl2、SO2、NO2)的性质.
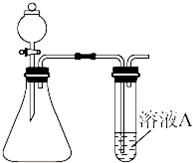 (1)装药品前,应先进行的操作
(1)装药品前,应先进行的操作
(2)如果用该装置制取H2、O2,可选用的试剂组合是 (填序号).
(3)五种气体中,可同时采用如图所示两种收集装置收集的气体是 .
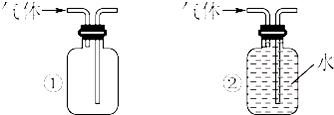
(4)两同学分别利用该装置制取并探究气体性质.同学甲利用亚硫酸钠固体与硫酸反应制取SO2,同学乙用高锰酸钾和盐酸制取氯气.请回答:
①写出亚硫酸钠固体与硫酸反应制取SO2的化学方程式: .
②若溶液A为溴水,通入SO2后现象是 ;若溶液A为溴化钠溶液,通入氯气时反应的离子方程式为 .实验证明Br2、SO2和Cl2氧化性由大到小的顺序为 .
③两同学想比较Cl2和SO2漂白速率的快慢,A溶液选取的是相同量的品红溶液.同时制取气体Cl2和SO2,观察品红溶液褪色的时间,比较褪色的快慢,该方法存在的缺陷为 .两同学还想比较Cl2和
SO2漂白的差异性,还需要的操作和可能观察到的现象为 .
 (1)装药品前,应先进行的操作
(1)装药品前,应先进行的操作(2)如果用该装置制取H2、O2,可选用的试剂组合是
| H2 | O2 | |
| ① | Zn、稀盐酸 | KClO3、MnO2 |
| ② | Zn、稀硫酸 | H2O2溶液、MnO2 |
| ③ | Zn、稀硝酸 | KMnO4 |
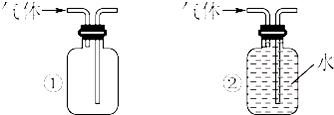
(4)两同学分别利用该装置制取并探究气体性质.同学甲利用亚硫酸钠固体与硫酸反应制取SO2,同学乙用高锰酸钾和盐酸制取氯气.请回答:
①写出亚硫酸钠固体与硫酸反应制取SO2的化学方程式:
②若溶液A为溴水,通入SO2后现象是
③两同学想比较Cl2和SO2漂白速率的快慢,A溶液选取的是相同量的品红溶液.同时制取气体Cl2和SO2,观察品红溶液褪色的时间,比较褪色的快慢,该方法存在的缺陷为
SO2漂白的差异性,还需要的操作和可能观察到的现象为