题目内容
6.有一瓶澄清的溶液,其中可能含有NH4+、K+、Na+、Mg2+、Al3+、Fe3+、Ba2+、Cl-、I-、NO3-、CO32-、SO42-中的几种.取该溶液进行以下实验:(1)用pH试纸检验该溶液呈强酸性,可推出CO32-离子不存在.
(2)取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡后CCl4层呈紫红色,可推出NO3-、Fe3+离子不存在.
(3)另取部分溶液,向其中逐滴加入NaOH溶液,使溶液从酸性逐渐变为碱性,在滴加过程中和滴加完毕后,均无沉淀产成,则可推出Mg2+、Al3+离子不存在.取部分碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝,说明NH4+离子存在.
(4)另取部分上述碱性溶液,向其中加入Na2CO3溶液,有白色沉淀生成,可推出SO42-离子不存在.
(5)根据以上实验事实确定:该溶液中肯定存在的离子是Ba2+、I-、NH4+;还不能肯定是否存在的离子是K+、Na+、Cl-.
分析 根据澄清溶液得,原溶液没有相互反应的离子;
(1)根据实验(1)溶液呈中性判断氢离子一定存在,与氢离子反应的离子不能够共存;
(2)根据实验(2)加入少量CCl4及数滴新制氯水,经振荡后CCl4层呈紫红色,说明溶液中一定含有碘离子,能够与碘离子反应的离子不共存;
(3)根据实验(3)加入NaOH溶液,使溶液从酸性逐渐变为碱性,在滴加过程中和滴加完毕后,溶液均无沉淀产判断凡是与氢氧根离子反应生成沉淀的离子不存在;
(4)根据实验(4)另取部分上述碱性溶液加Na2CO3溶液,有白色沉淀生成,可知一定含有碳酸根离子,排除与该离子反应的离子;
(5)由上述分析判断一定存在的离子、不能确定的离子.
解答 解:(1)根据实验(1)现象:溶液呈强酸性,说明溶液中肯定含有H+,而H+与CO32-反应发生反应而不能共存,说明溶液中肯定不含有CO32-,故答案为:CO32-;
(2)根据实验(2)现象:CCl4层呈紫红色,说明有I2,这是由于I-被氯气氧化所产生的,从而说明溶液中含有I-,而I-与Fe3+、NO3-和H+能发生氧化还原反应,而不能共存,说明溶液中肯定不含有Fe3+、NO3-;
故答案为:NO3-、Fe3+;
(3)根据实验(3)现象:溶液从酸性逐渐变为碱性,在滴加过程中和滴加完毕后,溶液均无沉淀产生,而Fe3+、Mg2+、Al3+能与碱反应产生沉淀,说明溶液中肯定不含有Mg2+、Al3+;取部分碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝,说明一定存在铵根离子.
故答案为:Mg2+、Al3+;NH4+;
(4)根据实验(4)现象:取出部分上述碱性溶液加Na2CO3溶液后,有白色沉淀生成,说明溶液中肯定含有Ba2+,而Ba2+能与SO42-产生沉淀,说明溶液中不含SO42-;
故答案为:SO42-;
(5)由上述实验事实确定,该溶液中肯定存在的离子是:Ba2+、I-、NH4+;肯定不存在的离子是:Mg2+、Fe3+、Al3+、NO3-、Fe3+、CO32-、SO42-;
还不能确定是否存在的离子是:K+、Na+、Cl-,
故答案为:Ba2+、I-、NH4+;K+、Na+、Cl-.
点评 本题考查物质的检验及鉴别,为高频考点,把握常见离子之间的反应、离子检验等为推断的关键,侧重分析与推断能力的综合考查,题目难度不大.

| A. | 2I-+Cl2═I2+2Cl- | B. | 2Br-+Cl2═Br2+2Cl- | ||
| C. | Br2+2I-═2Br-+I2 | D. | 2Fe2++I2═2Fe3++2I- |
| A. | 小于7 | B. | 小于5.6 | C. | 大于5.6 | D. | 小于0 |
| A. | CO2H2O | B. | C2H4 CH4 | C. | Cl2 C2H2 | D. | NH3HCl |
| A. | $\frac{4n-1}{2}$ | B. | $\frac{n-m}{3}$ | C. | $\frac{3m+n}{3}$ | D. | 3(n-m) |
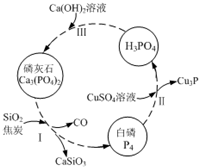 氮、磷及其化合物在科研及生产中均有着重要的应用.
氮、磷及其化合物在科研及生产中均有着重要的应用.