题目内容
分离物质应从物质状态和相关物理性质、化学性质角度出发,尽量用物理方法进行分离:
(1)固体和固体的分离方法有:①____________; ②____________; ③____________
(2)固体和液体的分离方法有:________。
(3)液体和液体的分离方法有: ①____________; ②____________; ③___________
(4)气体和气体的分离方法有:______________。
(1)固体和固体的分离方法有:①____________; ②____________; ③____________
(2)固体和液体的分离方法有:________。
(3)液体和液体的分离方法有: ①____________; ②____________; ③___________
(4)气体和气体的分离方法有:______________。
(1)①溶解、过滤(可溶与不可溶于水的物质混合);②蒸发、结晶(利用溶解度随温度变化的差异);③升华(如NaCl与I2的混合物)
(2)过滤
(3)①蒸馏(根据沸点的差异);②萃取(根据溶质在互不相溶的溶剂中溶解度的差异);③分液(互不相溶的液体)
(4)洗气
(2)过滤
(3)①蒸馏(根据沸点的差异);②萃取(根据溶质在互不相溶的溶剂中溶解度的差异);③分液(互不相溶的液体)
(4)洗气

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
(1)某同学为探究蔗糖的水解反应,进行如下实验,填写实验步骤III的实验现象:
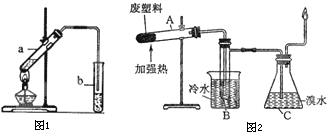
(2)“酒是陈的香”的原因之一是储存过程中生成了有香味的酯.实验室用下图所示装置制取乙酸乙酯.
①试管a中生成乙酸乙酯的化学反应方程式是 .
②试管b中盛放的试剂是 溶液
③若要把b中制得的乙酸乙酯从混合物中分离出来,应采用的实验操作是 .
④生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态.下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号) .
a单位时间里,生成1mol乙酸乙酯,同时生成1mol水
b单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
c单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
d正反应的速率与逆反应的速率相等
e混合物中各物质的浓度不再变化
(3)加热聚丙烯塑料得到的产物如表:
实验装置如图所示.
①试管A中的最终残余物为 ;
②试管B收集到的产品中,有能使酸性高锰酸钾溶液褪色的物质,该物质的一氯代物有 种.
③锥形瓶C中观察到的现象是 ;经溴水充分吸收再干燥后,剩余两种气体的平均相对分子质量为 .

| 实验步骤 | 实验现象 |
| I.向编号为①②③的3支试管中,分别加入1mL 20%的蔗糖溶液,向试管②和③中加入0.5mL稀硫酸,并将这3支试管同时水浴加热约5min | 均无明显现象 |
| II.取试管①和②,加入新制氢氧化铜悬浊液,加热至沸腾 | 均无明显现象 |
| III.取试管③,先加入NaOH溶液调溶液pH至碱性,再加入新制氢氧化铜悬浊液,加热至沸腾 | |
| 结论:证明蔗糖在稀硫酸作用下发生了水解反应 | |
①试管a中生成乙酸乙酯的化学反应方程式是
②试管b中盛放的试剂是
③若要把b中制得的乙酸乙酯从混合物中分离出来,应采用的实验操作是
④生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态.下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号)
a单位时间里,生成1mol乙酸乙酯,同时生成1mol水
b单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
c单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
d正反应的速率与逆反应的速率相等
e混合物中各物质的浓度不再变化
(3)加热聚丙烯塑料得到的产物如表:
| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
①试管A中的最终残余物为
②试管B收集到的产品中,有能使酸性高锰酸钾溶液褪色的物质,该物质的一氯代物有
③锥形瓶C中观察到的现象是
 O2(g)=CO2(g) △H= —283kJ/mol
O2(g)=CO2(g) △H= —283kJ/mol H2(g)+CO2(g)△H=
H2(g)+CO2(g)△H=  (CO)=
(CO)= (H2O) d.c(CO)=c(H2)
(H2O) d.c(CO)=c(H2) 
 (CO2)表示的反应速率为 。
(CO2)表示的反应速率为 。




 ,该分子中官能团的名称为
,可以和醇类物质发生
反应,还可以发生分子内脱水生成马来酸,马来酸能使溴水褪色,则马来酸的结构简式为 。
,该分子中官能团的名称为
,可以和醇类物质发生
反应,还可以发生分子内脱水生成马来酸,马来酸能使溴水褪色,则马来酸的结构简式为 。
