题目内容
【题目】熔融碳酸盐燃料电池(Molen Cathomale Fuel Cell)简称MCFC,具有高发电效率。工作原理示意图如图。下列说法正确的是
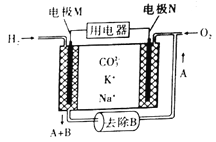
A. 电极M 为负极,K+、Na+移向M
B. 电池工作时,熔融盐中CO32-物质的量增大
C. A 为CO2,正极的电极反应为:O2+4e-+2CO2= 2CO32-
D. 若用MCFC给铅蓄电池充电,电极N接Pb极
【答案】C
【解析】氢氧燃料电池,氢气做负极,氧气为正极,电极M为负极,电解质中阳离子向正极移动,移向电极N,A错误;电极的负极反应为:2H2-4e-+2CO32-=2H2O+2CO2,电极的正极反应为:O2+4e-+2CO2=2CO32-,所以电池工作时,熔融盐中CO32-物质的量不变,B错误;正极发生还原反应,氧气在正极得电子,电极反应为:O2+4e-+2CO2=2CO32-,所以要通入CO2,C正确;铅蓄电池铅为负极,要与电源的负极相连接,因此要连接电源的M极;D错误;正确选项C。

【题目】下表是元素周期表中的一部分,根据①~⑨在周期表中的位置,用元素符号或化学式回答下列问题:
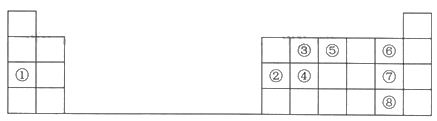
(1)元素④在元素周期表中的位置为________。
(2)最高价氧化物的水化物中碱性最强的物质的电子式为________。
(3)写出②和⑦两种元素的最高价氧化物的水化物相互反应的化学方程式:_______。
(4)④、⑤、⑥三种元素按原子半径由大到小的顺序排列为_______。
(5)③和⑦两种元素形成的简单化合物的结构式为_______,空间构型为________。
(6)设计实验探究⑦、⑧两种元素非金属性的相对强弱。
可选用的试剂有:氯水、NaBr溶液、AgNO3溶液、苯。
请完成实验报告单。
步骤一 | 步骤二 | |
实验内容 | 试管1:取少量氯水; 试管2:取少量氯水,滴加少量NaBr溶液。 | 分别向试管1、试管2中加少量______(填试剂),振荡,静置。 |
实验现象 | 试管2中的现象是______。 | 试管2中的现象是_______。 |
实验分析 | 试管1的作用是_____。 | 试管2中反应的离子方程式为_____,此实验的结论是_____。 |

