题目内容
向一固定体积的密闭容器中通入amol的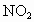 气体,在一定条件下发生反应:
气体,在一定条件下发生反应: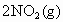
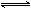
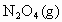 .达到平衡后若再通入
.达到平衡后若再通入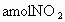 气体,再次达平衡时,
气体,再次达平衡时,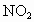 的转化率比第一次达平衡时的转化率________(填“大”或“小”).若
的转化率比第一次达平衡时的转化率________(填“大”或“小”).若
开始通入的为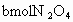 ,气体,在密闭容器发生反应;.达到平衡时再通入bmol的
,气体,在密闭容器发生反应;.达到平衡时再通入bmol的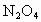 气体,再次达平衡时
气体,再次达平衡时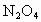 的转化率比第一次达平衡时的转化率________(填“大”或“小”).
的转化率比第一次达平衡时的转化率________(填“大”或“小”).
解析:
|
对于含两种以上反应物的平衡体系,若增加一种反应物的浓度,则另外反应物的转化率增大而本身转化率反而会减小.若只有一种反应物,且反应前后气体分子系数之和不等时,则再加入反应物时,其转化率可能增大也可能减小:当正反应是气体体积减小时转化率增大,当正反应是气体体积增加时转化率减小.题中容器的体积设为 V升,开始加入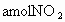 时,平衡后转化率设为x%,当再通入 时,平衡后转化率设为x%,当再通入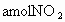 气体,再建立平衡时转化率设为y%.此时最终的平衡可转换为这样的建立途径:将 气体,再建立平衡时转化率设为y%.此时最终的平衡可转换为这样的建立途径:将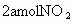 气体通入2V升的密闭容器中达平衡时, 气体通入2V升的密闭容器中达平衡时,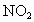 的转化率应为x%;再将容器压缩至V升,达平衡时, 的转化率应为x%;再将容器压缩至V升,达平衡时,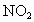 的转化率应为y%;而在压缩的过程中,平衡向气体体积缩小的正反应方向移动,故转化率增大,即y>x.反过来,若开始通入的为 的转化率应为y%;而在压缩的过程中,平衡向气体体积缩小的正反应方向移动,故转化率增大,即y>x.反过来,若开始通入的为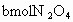 气体,平衡时的转化率设为m%,当再通入 气体,平衡时的转化率设为m%,当再通入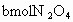 气体,建立平衡时转化率设为n%;此时最终的平衡可转换为这样的建立途径:将2bmol的 气体,建立平衡时转化率设为n%;此时最终的平衡可转换为这样的建立途径:将2bmol的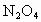 气体通入2V升的密闭容器中达平衡时, 气体通入2V升的密闭容器中达平衡时,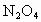 的转化率应为m%;再将容器压缩至V升,达平衡时 的转化率应为m%;再将容器压缩至V升,达平衡时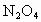 的转化率应为n%.而压缩过程中,平衡要向气体体积缩小的逆反应方向移动,故 的转化率应为n%.而压缩过程中,平衡要向气体体积缩小的逆反应方向移动,故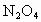 的转化率减小,即m>n. 的转化率减小,即m>n. |

 全能测控期末小状元系列答案
全能测控期末小状元系列答案(1)在一定体积的密闭容器中,进行如下化学反应,CO2(g)+H2(g)![]() CO(g)+H2O(g)。其化学平衡常数K与温度t的关系如下。请回答下列问题:
CO(g)+H2O(g)。其化学平衡常数K与温度t的关系如下。请回答下列问题:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
①该反应的化学平衡常数的表达式K = ,由上表数据可得,该反应为 反应。(填“吸热”或“放热”)
②800℃,固定容器的密闭容器中,放入混合物,其始浓度为c(CO)=0.01 mol·L-1、c(H2O)=0.03mol·L-1、c(CO2)=0.01 mol·L-1、c(H2)=0.05 mol·L-1,则反应开始时,H2O的消耗速率比生成速率 (填"大"、"小"或"不能确定")
③830℃,在1 L的固定容器的密闭容器中放入2 mol CO2和1 mol H2,平衡后CO2的转化率为 。
(2)目前工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验,在体积为1L的密闭容器中,充入1mol CO2和3mol H2,在500℃下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H=-49.0kJ·mol-1。测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示:
CH3OH(g)+H2O(g) △H=-49.0kJ·mol-1。测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示:
①平衡时CH3OH的体积分数w为 。
②现在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下。下列说法正确的是
| 容器 | 实验1 | 实验2 | 实验3 |
| 反应物投入量(始态) | 1mol CO2、3mol H2 | 1mol CH3OH、1mol H2O | 2mol CH3OH、2mol H2O |
| CH3OH的平衡浓度/mol·L-1 | C1 | C2 | C3 |
| 反应的能量变化 | 放出 x kJ | 吸收y kJ | 吸收z kJ |
| 体系压强/Pa | P1 | P2 | P3 |
| 反应物转化率 | a1 | a2 | a3 |
A.2 C1>C3 B.x+y=49.0 C.2P2<P3
D.(a1+a3)<1 E.2P1>P3 F.a1= a2
③在一个装有可移动活塞的容器中进行上述反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。反应达到平衡后,测得CH3OH的物质的量为a mol,保持容器内的温度和压强不变,向平衡体系中通入少量的H2,再次达到平衡后,测得CH3OH的物质的量为b mol,请比较a、b的大小 。
CH3OH(g)+H2O(g)。反应达到平衡后,测得CH3OH的物质的量为a mol,保持容器内的温度和压强不变,向平衡体系中通入少量的H2,再次达到平衡后,测得CH3OH的物质的量为b mol,请比较a、b的大小 。
(14分)研究CO2的利用对促进低碳社会的构建具有重要的意义。
⑴ 在一定体积的密闭容器中,进行化学反应: CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)
其化学平衡常数K和温度t的关系如下表:
①该反应正向反应是 反应。(填“放热”或“吸热”)
②能判断该反应达到化学平衡状态的依据是 。
| A.容器压强不变 | B.混合气体中c(CO2)不变 | C.υ正(H2)=υ逆(H2O) | D.c(CO2)=c(CO) |
⑵工业上合成甲醇可在密闭容器中采用如下反应进行:
CO2(g) +3H2(g)
 CH3OH(g) +H2O(g) △H=-49.0 kJ·mol-1
CH3OH(g) +H2O(g) △H=-49.0 kJ·mol-1 ①该反应的平衡常数表达式K= 。
②某实验将1molCO2和3molH2充入一定体积的密闭容器中,在两种不同条件下发生反应(只有一种条件不同)。测得CH3OH的物质的量随时间变化如图所示:

曲线I、Ⅱ对应的平衡常数大小关系为KⅠ KⅡ(选填“>”、“=”或“<”)。
③一定温度下,在容积2L且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
| 容 器 | 甲 | 乙 |
| 反应物投入量 | 1molCO2、3molH2 | a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) |
要使平衡后乙容器与甲容器中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则c的取值范围为 。
(1)在一定体积的密闭容器中,进行如下化学反应,CO2(g)+H2(g) CO(g)+H2O(g)。其化学平衡常数K与温度t的关系如下。请回答下列问题:
CO(g)+H2O(g)。其化学平衡常数K与温度t的关系如下。请回答下列问题:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
①该反应的化学平衡常数的表达式K = ,由上表数据可得,该反应为 反应。(填“吸热”或“放热”)
②800℃,固定容器的密闭容器中,放入混合物,其始浓度为c(CO)="0.01" mol·L-1、c(H2O)="0.03" mol·L-1、c(CO2)="0.01" mol·L-1、c(H2)="0.05" mol·L-1,则反应开始时,H2O的消耗速率比生成速率 (填"大"、"小"
 或"不能确定")
或"不能确定")③830℃,在1 L的固定容器的密闭容器中放入2 mol CO2和1 mol H2,平衡后CO2的转化率为 。
(2)目前工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验,在体积为1L的密闭容器中,充入1mol CO2和3mol H2,在500℃下发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O
CH3OH(g)+H2O (g) △H=-49.0kJ·mol-1。测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示:
(g) △H=-49.0kJ·mol-1。测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示:
①平衡时CH3OH的体积分数w为 。
②现在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数
 据如下。下列说法正确的是
据如下。下列说法正确的是 | 容器 | 实验1 | 实验2 | 实验3 |
| 反应物投入量(始态) | 1mol CO2、3mol H2 | 1mol CH3OH、1mol H2O | 2mol CH3OH、2mol H2O |
| CH3OH的平衡浓度/mol·L-1 | C1 | C2 | C3 |
| 反应的能量变化 | 放出 x kJ | 吸收y kJ | 吸收z kJ |
| 体系压强/Pa | P1 | P2 | P3 |
| 反应物转化率 | a1 | a2 | a3 |
D.(a1+ a3)<1 E.2P1> P3 F.a1= a2
③在一个装有可移动活塞的容器中进行上述反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。反应达到平衡后,测得CH3OH的物质的量为a mol,保持容器内的温度和压强不变,向平衡体系中通入少量的H2,再次达到平衡后,测得CH3OH的物质的量为b mol,请比较a、b的大小 。
CH3OH(g)+H2O(g)。反应达到平衡后,测得CH3OH的物质的量为a mol,保持容器内的温度和压强不变,向平衡体系中通入少量的H2,再次达到平衡后,测得CH3OH的物质的量为b mol,请比较a、b的大小 。 (14分)研究CO2的利用对促进低碳社会的构建具有重要的意义。
⑴ 在一定体积的密闭容器中,进行化学反应: CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)
其化学平衡常数K和温度t的关系如下表:

①该反应正向反应是 反应。(填“放热”或“吸热”)
②能判断该反应达到化学平衡状态的依据是 。
A.容器压强不变 B.混合气体中c(CO2)不变
C.υ正(H2)=υ逆(H2O) D.c(CO2)=c(CO)
③当其他条件不变时,若缩小容器的体积,该反应平衡 移动。(选填“正向”、“逆向”或“不”)
⑵工业上合成甲醇可在密闭容器中采用如下反应进行:
CO2(g) +3H2(g)  CH3OH(g) +H2O(g)
△H=-49.0 kJ·mol-1
CH3OH(g) +H2O(g)
△H=-49.0 kJ·mol-1
①该反应的平衡常数表达式K= 。
②某实验将1molCO2和3molH2充入一定体积的密闭容器中,在两种不同条件下发生反应(只有一种条件不同)。测得CH3OH的物质的量随时间变化如图所示:

曲线I、Ⅱ对应的平衡常数大小关系为KⅠ KⅡ(选填“>”、“=”或“<”)。
③一定温度下,在容积2L且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
|
容 器 |
甲 |
乙 |
|
反应物投入量 |
1molCO2、3molH2 |
a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) |
经测定甲容器经过5min达到平衡,平衡时CO2的转化率为50%,甲容器中该反应在5min内的平均速率υ(H2)= mol·L-1·min-1。
要使平衡后乙容器与甲容器中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则c的取值范围为 。
 研究CO2的利用对促进低碳社会的构建具有重要的意义.
研究CO2的利用对促进低碳社会的构建具有重要的意义.