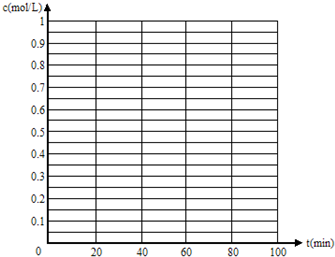
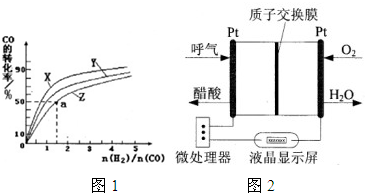
题目内容
在体积为2L的密闭容器中,CO与H2在一定条件下反应生成甲醇:
CO(g)+2H2(g)

CH3OH(g).反应达到平衡时,平衡常数表达式K=______,升高温度,K值______(填“增大”、“减小”或“不变”).在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=______.
CO(g)+2H2(g)

CH3OH(g).反应达到平衡时,平衡常数表达式K=______,升高温度,K值______(填“增大”、“减小”或“不变”).在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=______.

因化学平衡常数等于生成物的浓度系数次幂之积除以反应物的浓度系数次幂之积,所以K=
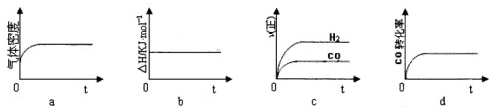
,由图可知,升高温度,甲醇的含量降低,平衡逆向移动,
则化学平衡常数减小,由图象可知,在500℃时,2min到达平衡,甲醇的平均反应速率v(CH3OH)=
=0.05mol?(L?min)-1,由速率之比等于化学计量数之比求出,
则v(H2)=2v(CH3OH)=2×0.05mol?(L?min)-1=0.1mol?(L?min)-1;
故答案为:
;减小;0.1mol?(L?min)-1.
| c(CH3OH) |
| c(CO)c2(H2) |
则化学平衡常数减小,由图象可知,在500℃时,2min到达平衡,甲醇的平均反应速率v(CH3OH)=
| ||
| 2min |
则v(H2)=2v(CH3OH)=2×0.05mol?(L?min)-1=0.1mol?(L?min)-1;
故答案为:
| c(CH3OH) |
| c(CO)c2(H2) |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 Ⅰ:如图表示800℃时,A、B、C三种气体物质的浓度随时间的变化情况,t1是达到平衡状态的时间.试回答:
Ⅰ:如图表示800℃时,A、B、C三种气体物质的浓度随时间的变化情况,t1是达到平衡状态的时间.试回答: