题目内容
|
1 g O2含有m个氧分子,则阿伏加德罗常数的数值可表示为 | |
| [ ] | |
A. |
m/32 |
B. |
m/16 |
C. |
32m |
D. |
16m |
解析:
|
1 g O2的物质的量为1 g/32(g·mol-1)=1/32 mol.因此阿伏加德罗常数NA=32m. |

(15分)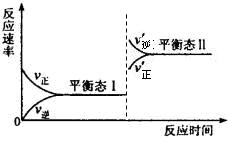
物质A、B、C有如下转化关系:
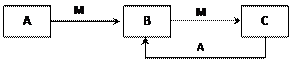 |
请回答下列问题:
(1)若A、B、C均为含铝元素的化合物,M的化学式可以是 。
(2)若M是第IVA族某元素的最高价氧化物,且M为气体,组成A的阴阳离子均含有10个电子,C的化学式是 ,请写出C的一种用途 。
(3)若A是一种黄绿色气体,M是一种常见金属。写出C→B的离子方程式
。
(4)若A、B、C都是含硫化合物,已知:
A转化为B的热化学方程式为:2H2S(g)+ O2(g) =2S (s)+2H2O(l) △H=" -a" kJmol-1;
A转化为C的热化学方程式为:2H2S(g)+ 3O2(g) =2SO2(g)+2H2O(l) △H="-b" kJmol-1;
请写出A与C反应转化为B的热化学方程式 。
(5)若C+A→B的转化关系为4NH3+6NO
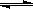 6H2O+5N2。在一定条件下,该反应达到平衡态I后,升高温度平衡发生移动,达到平衡态II的反应速率随时间变化的关系图如右。该反应为 (填“吸热”或“放热”)反应;升高温度,该反应的平衡常数K值 (填“增大”、“减小”或“不变”)
6H2O+5N2。在一定条件下,该反应达到平衡态I后,升高温度平衡发生移动,达到平衡态II的反应速率随时间变化的关系图如右。该反应为 (填“吸热”或“放热”)反应;升高温度,该反应的平衡常数K值 (填“增大”、“减小”或“不变”) (14分)X、Y、Z、W是元素周期表中前四周期的常见元素,其相关信息如下表;
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 原子最外层电子数是次外层的三倍 |
| Z | 单质及其化合物的焰色反应为黄色 |
| W | W元素基态原子的M层全充满,N层只有一个电子 |
 。X的一种单质熔点很高,硬度很大,则这种单质的晶体属于 晶体。
。X的一种单质熔点很高,硬度很大,则这种单质的晶体属于 晶体。⑵ X与Y中电负性较强的是(填元素符号) ;XY2的电子式是 ,分子中存在 个σ键。
⑶Z2Y2中含有的化学键类型有 。阴、阳离子的个数比为 。
⑷W的基态原子核外电子排布式是 。
⑸废旧印刷电路板上有W的单质A。用H2O2和H2SO4的混合溶液可溶出印刷电路板上的A。已知:
A(s)+H2SO4(aq) ="=" ASO4(aq) + H2(g) ΔH=+64.4kJ·mol-1
2H2O2(l) ="=" 2H2O(l) + O2(g) ΔH= -196.4kJ·mol-1
H2(g)+
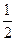 O2(g) ="=" H2O(l) ΔH= -285.8kJ·mol-1
O2(g) ="=" H2O(l) ΔH= -285.8kJ·mol-1请写出A与H2SO4、H2O2反应生成ASO4(aq)和H2O(l)的热化学方程式(A用化学式表示):
。
(14分)X、Y、Z、W是元素周期表中前四周期的常见元素,其相关信息如下表;
|
元素 |
相关信息 |
|
X |
X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
|
Y |
原子最外层电子数是次外层的三倍 |
|
Z |
单质及其化合物的焰色反应为黄色 |
|
W |
W元素基态原子的M层全充满,N层只有一个电子 |
⑴ X位于元素周期表第 族。X的一种单质熔点很高,硬度很大,则这种单质的晶体属于 晶体。
⑵ X与Y中电负性较强的是(填元素符号) ;XY2的电子式是 ,分子中存在 个σ键。
⑶Z2Y2中含有的化学键类型有 。阴、阳离子的个数比为 。
⑷W的基态原子核外电子排布式是 。
⑸废旧印刷电路板上有W的单质A。用H2O2和H2SO4的混合溶液可溶出印刷电路板上的A。已知:
A(s)+H2SO4 (aq) == ASO4(aq) + H2(g) ΔH=+64.4kJ·mol-1
2H2O2(l) == 2H2O(l) + O2(g) ΔH= -196.4kJ·mol-1
H2(g)+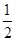 O2(g) == H2O(l) ΔH= -285.8kJ·mol-1
O2(g) == H2O(l) ΔH= -285.8kJ·mol-1
请写出A与H2SO4、H2O2反应生成ASO4(aq)和H2O(l)的热化学方程式(A用化学式表示):
。
 (2011?安徽模拟)如图所示,隔板K1固定不动,活塞K2可自由移动.T℃时,M、N两个容器中均发生反应2SO2(g)+O2(g)?2SO3(g),向容器M、N中各充入2mol SO2和1mol O2,初始M、N的容积和温度相同,并保持温度不变.下列有关说法中不正确的是( )
(2011?安徽模拟)如图所示,隔板K1固定不动,活塞K2可自由移动.T℃时,M、N两个容器中均发生反应2SO2(g)+O2(g)?2SO3(g),向容器M、N中各充入2mol SO2和1mol O2,初始M、N的容积和温度相同,并保持温度不变.下列有关说法中不正确的是( )