题目内容
5.下列说法正确的是( )| A. | 海水提溴的过程中不发生氧化还原反应 | |
| B. | 铁的冶炼过程是利用置换反应得到单质铁 | |
| C. | 石油分馏是物理变化,可得到汽油、煤油和柴油等 | |
| D. | CO2、NO2或者SO2都会导致酸雨的形成 |
分析 A.溴离子变为溴单质为氧化还原反应;
B.工业上用一氧化碳还原氧化铁;
C.分馏是根据沸点不同进行分离;
D.二氧化碳不导致酸雨.
解答 解:A.溴离子失电子发生氧化反应而生成溴单质,所以发生了氧化还原反应,故A错误;
B.工业上用一氧化碳还原氧化铁生成铁和二氧化碳,所以不是置换反应,故B错误;
C.分馏是根据混合物的沸点不同进行分离,为物理变化,故C正确;
D.二氧化碳可导致温室效应,NO2或者SO2都会导致酸雨,故D错误.
故选C.
点评 本题考查较为综合,涉及氧化还原反应、金属的冶炼、物质的分离以及环境保护等问题,侧重于化学与生活、生产和环保问题,有利于培养学生的良好的科学素养,提高学习的积极性,难度不大.

练习册系列答案
相关题目
15.分类是科学研究的重要方法,下列物质分类不正确的是( )
| A. | 非电解质:乙醇,氯气,乙酸 | |
| B. | 醇:甘油,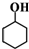 , ,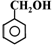 | |
| C. | 分子晶体:干冰,碘单质,蔗糖 | |
| D. | 混合物:铝热剂,聚乙烯,分析纯盐酸 |
13.已知反应2A?B+3C,在20℃进行时其v(A)=5mol•L-1•s-1.如果温度每升高10℃,此反应速率增大到原来的2倍.则当其他条件不变时,温度升至50℃时,此反应的化学反应速率v(C)是( )
| A. | 20 mol•L-1•s-1 | B. | 40 mol•L-1•s-1 | C. | 60 mol•L-1•s-1 | D. | 150mol•L-1•s-1 |
20.在盛有稀H2SO4的烧杯中放入用导线连接的锌片和铜片,下列叙述错误的是( )
| A. | 负极附近SO42- 逐渐增大 | |
| B. | 电子通过导线由铜片流向锌片 | |
| C. | 反应一段时间后,溶液的H+浓度降低 | |
| D. | 铜片上有H2逸出 |
17.下列实验中没有颜色变化的是( )
| A. | 葡萄糖溶液与新制的Cu(OH)2悬浊液混合加热 | |
| B. | 木板上涂抹浓硫酸 | |
| C. | 淀粉溶液中加入碘酒 | |
| D. | 苯加入到酸性高锰酸钾溶液中 |
14.对下列图象的描述中,正确的是( )
| A. |  根据图可判断正反应的△H<0 | |
| B. |  根据图,除去CuSO4溶液中的Fe3+,可加入CuO调节pH至3~5 | |
| C. | 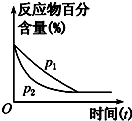 图可表示压强(p)对反应2A(g)+2B(g)?3C(g)+D(s)的影响 | |
| D. |  图为水的电离平衡曲线图,若从A点到C点,可采用在水中加入适量NaOH固体的方法 |
15.用水就能鉴别的一组物质是( )
| A. | 乙烯、乙炔 | B. | 乙酸、乙醛 | C. | 苯、甲苯 | D. | 己烷、乙醇 |
 、⑤ClCH=CHCl⑥
、⑤ClCH=CHCl⑥ 、⑦
、⑦ 、⑧
、⑧ 、⑨
、⑨

 (或
(或 )
)

 溶解性由大到小的顺序
溶解性由大到小的顺序