题目内容
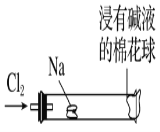
【题目】按下图装置进行实验,并回答下列问题:

(1)判断装置的名称:A池为___________ ;B池为______________;
(2)锌极为________极,电极反应式为___________________________________;铜极为________极,电极反应式为___________________________________;石墨棒C1为______极,电极反应式为__________________________________;石墨棒C2附近发生的实验现象为______________________________________;
(3)当C2极析出224mL气体(标准状态)时,锌的质量变化_________(变大、不变或变小)了________g,CuSO4溶液的质量_________(增加、不变或减少)_________g。
【答案】原电池 电解池 负极 Zn—2e-=Zn2+ 正极 Cu2++2e-=Cu 阳极 2Cl--2e-=Cl2↑ 溶液呈红色 变小 0.65 增加 0.01
【解析】
(1)由题给装置可知,A为原电池,B为电解池;
(2)A为原电池,金属活泼性较强的锌为负极,电极反应式为Zn-2e-=Zn2+;金属活泼性较弱的铜为正极,电极反应为:Cu2++2e-=Cu,石墨棒C1与原电池的正极相连为电解池的阳极,阳极上氯离子失电子生成氯气,电极反应式为:2Cl--2e-=Cl2↑;石墨棒C2与原电池的负极相连为电解池的阴极,电极反应式为2H++2e-=H2↑,阴极附近生成氢气和氢氧根离子,溶液呈变红;
(3)石墨棒C2与原电池的负极相连为电解池的阴极,电极反应式为2H++2e-=H2↑,当C2极析出224mL气体(标准状况)时,生成氢气的物质的量为0.01mol,转移的电子为0.02mol,锌电极的方程式为:Zn-2e-=Zn2+,根据电子守恒可知,消耗的Zn为0.01mol,则锌的质量减少0.65g,生成铜的物质的量为0.01mol,质量为6.4g,硫酸铜溶液质量增加0.01g。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】按要求回答下列问题:
(1)甲醇是一种重要的化工原料,有着重要的用途和应用前景。工业上一般采用下列两种反应合成甲醇:
反应I:CO(g)+2H2(g)CH3OH(g);△H1
反应II:CO2(g)+3H2(g)CH3OH(g)+H2O(g);△H2
①上述反应中原子利用率百分之百的是______(填“I”或“Ⅱ”)
②下表所列数据是反应I在不同温度下的化学平衡常数(K)
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
由表中数据判断△H1______0,T℃时,将2molCO和6molH2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol/L,此时T为______。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H1=-1275.6kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H2=-566.0kJ/mol
③H2O(g)=H2O(l)△H3=-44.0kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:______。