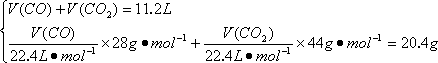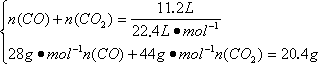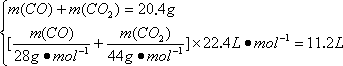题目内容
在标准状况下,11.2 L CO和CO2混合气体质量为20.4 g,求混合气体中CO和CO2的体积比和质量比.
答案:
解析:
解析:
|
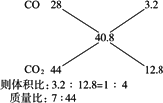
解答:本题有多种解法. 解法一:设原混合气体中CO、CO2的体积分别是V(CO)、V(CO2),则: 解出V(CO)=22.4 L,V(CO2)=8.96 L. 体积比: 质量比:(0.1×28)∶(0.4×44)=7∶44. 解法二:设混合气体中CO和CO2的物质的量分别是n(CO)、n(CO2). 解出n(CO)=0.1 mol;n(CO2)=0.4 mol. 体积比即物质的量之比:1∶4. 质量比:(0.1×28)∶(0.4×44)=7∶44. 解法三:设混合气体中CO和CO2的质量分别是m(CO)、m(CO2). 解出m(CO)=2.8 g,m(CO2)=17.6 g, 质量比:2.8∶17.6=7∶44, 体积比:0.1∶0.4=1∶4. 解法四:设混合气体平均相对分子质量为M,体积分数CO为x%,CO2为(1-x%). ①求出混合物的平均相对分子质量: 所以 ②求体积分数:x%×28+(1-x%)×44=40.8, x%=20%,CO2为80%, 体积比为1∶4. ③求质量比:(28×1)∶(4×44)=7∶44. 解法五:求出混合气体的平均相对分子质量为40.8.利用十字交叉法直接求解.
|

练习册系列答案
相关题目