题目内容
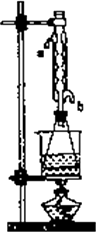
如图是制取乙酸乙酯的装置,下列说法中错误的是( )
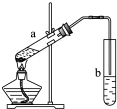

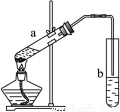
| A、浓硫酸在此反应中作为催化剂、吸水剂 | B、b中导气管不能插入饱和碳酸钠溶液中,目的是防止倒吸 | C、试管a中加入碎瓷片目的是防止剧烈沸腾 | D、先向试管a中加入浓硫酸,然后依次加入酒精、乙酸 |
分析:A.乙酸乙酯的反应中,浓硫酸的作用为吸水剂和催化剂;
B.若导管深入到液面以下,容易发生倒吸现象;
C.混合液体在受热时,容易发生暴沸现象,需要加入碎瓷片防止暴沸;
D.浓硫酸密度大,应将浓硫酸加入到乙醇中,以防酸液飞溅,乙酸易挥发,冷却后再加入乙酸.
B.若导管深入到液面以下,容易发生倒吸现象;
C.混合液体在受热时,容易发生暴沸现象,需要加入碎瓷片防止暴沸;
D.浓硫酸密度大,应将浓硫酸加入到乙醇中,以防酸液飞溅,乙酸易挥发,冷却后再加入乙酸.
解答:解:A.浓硫酸在乙酸乙酯的制取中起到的作用有催化剂、吸水剂,故A正确;
B.导管不能插入溶液中,导管要插在饱和碳酸钠溶液的液面上,伸入液面下可能发生倒吸,故B正确;
C.液体乙酸乙醇沸点低,加热时容易发生暴沸,所以要加碎瓷片,防止暴沸,故C正确;
D.为防止酸液飞溅,应将密度大的液体加入到密度小的液体中,乙酸易挥发,冷却后再加入乙酸,故D错误;
故选D.
B.导管不能插入溶液中,导管要插在饱和碳酸钠溶液的液面上,伸入液面下可能发生倒吸,故B正确;
C.液体乙酸乙醇沸点低,加热时容易发生暴沸,所以要加碎瓷片,防止暴沸,故C正确;
D.为防止酸液飞溅,应将密度大的液体加入到密度小的液体中,乙酸易挥发,冷却后再加入乙酸,故D错误;
故选D.
点评:本题考查了乙酸乙酯的制取方法,题目难度不大,注意掌握乙酸乙酯的制取原理,明确反应中浓硫酸、饱和碳酸钠溶液、碎瓷片的作用;选项D为易错点,注意制取混酸的正确操作方法.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
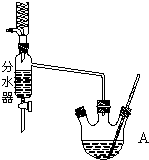 如图为制取乙酸乙酯的实验装置图.回答下列问题:
如图为制取乙酸乙酯的实验装置图.回答下列问题: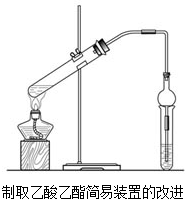 现用如图装置制取乙酸乙酯.请回答:
现用如图装置制取乙酸乙酯.请回答: