题目内容
1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度![]() ,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室中可以用下图所示装置制备1,2-二溴乙烷.其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水).
,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室中可以用下图所示装置制备1,2-二溴乙烷.其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水).
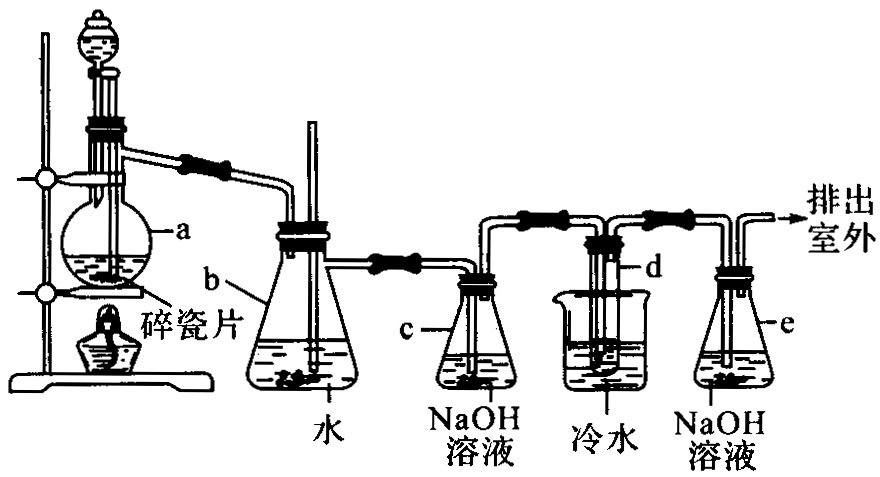
填写下列空白:(1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式_____________________________________________.
(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞.请写出发生堵塞时瓶b中的现象______________________.
(3)容器c中![]() 溶液的作用是__________________.
溶液的作用是__________________.
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多.如果装置的气密性没有问题,试分析其可能的原因.
解析:
|
答案:(1) (2)b中水面会下降,玻璃管中的水柱会上升,甚至溢出. (3)除去乙烯中带出的酸性气体(或除去 (4)①乙烯发生(或通过液溴)速度过快,②反应器a中的温度控制不当. 解析:因为分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,且在碎瓷片存在的条件下加热,并用温度计控制反应温度,结合教材中制乙烯的演示实验可知,该装置是乙烯气体的发生装置. 在反应器a中,可能发生的反应有: ① ② ③ ④ 其中②是本题有用的,也是希望发生的反应,顺着气流方向进行,进入容器c中的气体可能有乙烯、乙醚、
由于1,2-二溴乙烷的熔点为9.79℃(已知),故在冷水的冷却下,可能以固体存在,故试管d中的长导管可能堵塞.一旦发生堵塞,则会使容器b中的气体压强增大,水面下降,从而出现b中长导管(用以调节压强,防止倒吸)中水往迅速上升,甚至溢出.故b瓶起安全和缓冲气流的作用,可使气流较平稳. 由于有机反应通常具有反应速率慢、反应不够充分等特点,所以某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多,其中至少有以下两个原因具有可能性:①反应器a中的温度控制不当.如未能迅速升温到170℃,则会因发生生成乙醇的副反应,而使混合液损耗;如温度太高,则浓 |

 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案 ,主要制取1,2-二溴乙烷.则题中制备1,2-二溴乙烷的两个化学方程式为:
,主要制取1,2-二溴乙烷.则题中制备1,2-二溴乙烷的两个化学方程式为:





