题目内容
一密闭烧瓶中装有NO2气体,在一定条件下达到化学平衡2NO2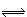 N2O4(正反应为放热反应)。将该烧瓶放在热水中,对现象的描述正确的是
N2O4(正反应为放热反应)。将该烧瓶放在热水中,对现象的描述正确的是
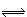 N2O4(正反应为放热反应)。将该烧瓶放在热水中,对现象的描述正确的是
N2O4(正反应为放热反应)。将该烧瓶放在热水中,对现象的描述正确的是 | A.颜色不变 | B.颜色变浅 | C.颜色加深 | D.无法判断 |
C
略

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
题目内容
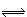 N2O4(正反应为放热反应)。将该烧瓶放在热水中,对现象的描述正确的是
N2O4(正反应为放热反应)。将该烧瓶放在热水中,对现象的描述正确的是 | A.颜色不变 | B.颜色变浅 | C.颜色加深 | D.无法判断 |

 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案