题目内容
|
下列叙述中正确的是 | |
| [ ] | |
A. |
氯化钠溶液中,氯化钠在电流的作用下电离成钠离子或氯离子 |
B. |
溶于水后能电离出氢离子的化合物都是酸 |
C. |
硫酸钡难溶于水,但硫酸钡是强电解质 |
D. |
SO2溶于水后部分电离,故二氧化硫属于弱电解质 |
答案:C
解析:
提示:
解析:
|
A项不正确,氯化钠溶液中,氯化钠在水分子的作用下电离成钠离子或氯离子;B项不正确,溶于水后能电离出的阳离子全部是氢离子的化合物称为酸;C项强弱电解质的定义与物质的溶解性无关,仅与在水中的电离程度有关,硫酸钡难溶于水,但硫酸钡溶解的部分能完全电离是强电解质;D项SO2溶于水后生成的H2SO3是弱电解质,能电离,但SO2本身不能电离,是非电解质,D不正确. |
提示:
|
1.划分强电解质和弱电解质的唯一标准是电解质能否完全电离. 2.电解质的强弱与溶液的导电性强弱也不是完全相关的.电解质溶液导电能力强弱主要取决于相同条件下溶液中自由移动离子的多少.强电解质稀溶液中离子的浓度不一定比弱电解质浓溶液中的离子浓度大,因而导电性不一定强. 3.电解质的强弱与物质的溶解性不是完全相关的.难溶性盐(如CaCO3、BaSO4等)在水中的溶解度极小,导电能力很小,但由于它们是离子化合物,在水溶液中溶解的那部分能完全电离,故它们属于强电解质.CH3COOH虽可与水以任意比混溶,却是弱电解质;C2H5OH虽可与水以任意比混溶,却是非电解质. 4.强、弱电解质溶液中,溶质的存在形式不同.强电解质溶液中溶质的存在形式是阴、阳离子,弱电解质溶液中除阴、阳离子外,还大量存在溶质的分子. |

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
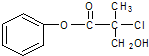 有机物A是农药生产中的一种中间体,结构简式如图所示.下列叙述中正确的是( )
有机物A是农药生产中的一种中间体,结构简式如图所示.下列叙述中正确的是( )| A、有机物A可以在一定条件下与HBr发生反应 | B、1mol A最多能与4mol H2发生加成反应 | C、有机物A与浓硫酸混合加热,可以发生消去反应 | D、1mol A与足量的NaOH溶液反应,最多可以消耗3mol NaOH |


