题目内容
一密封体中发生下列反应N2+3H2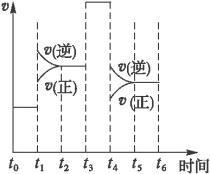
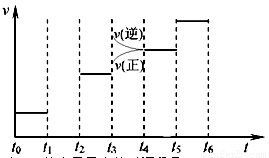
(1)处于平衡状态的时间段是_______________________。
(2)t1、t3、t4时刻,体系中分别是什么条件发生了变化?
(3)下列时间段中,氨的百分含量最高的是___________________。
A.t0—t1 B.t2—t3 C.t3—t4 D.t5—t6
(1)t0—t1、t2—t3、t3—t4、t5—t6
(2)t1时升高温度,t3时加了催化剂,t4时降低压强。
(3)A
解析:本题是考查反应速率与化学平衡内在联系的一道好题。通过做本题,掌握正确识别综合图象的方法思路。
从图中可以看出:t0—t1时间段内反应处于平衡状态。t1时刻,条件变化使正、逆反应速率加快,且逆反应速率大于正反应速率,平衡向逆反应方向移动,对照反应的特点及影响速率和平衡的规律,改变的条件应是“升高温度”。t3时刻时,正、逆反应速率都有同幅度的加快,应是“加了催化剂”。t4时刻时,正、逆反应速率都减慢,且Δv(正)>Δv(逆),平衡逆移,所以是由“降低压强”引起的。
由于t1—t2时间段和t3—t4时间段中,平衡都是向逆反应方向移动,氨的百分含量都减小,所以应是t0至t1时间段中氨的百分含量最高。

练习册系列答案
相关题目
 2NH3(g);△H<0 。
2NH3(g);△H<0 。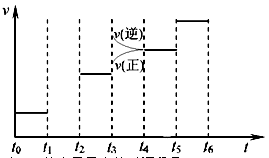
 2NH3(g);△H<0 。
2NH3(g);△H<0 。