题目内容
下列离子方程式中,正确的是
- A.将少量铜屑放入浓硝酸中:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
- B.氯气与水反应:Cl2+H2O=2H++Cl-+ClO-
- C.向氯化亚铁溶液中通入氯气:Fe2++Cl2=Fe3++2Cl-
- D.将氨气通入盐酸中:NH3+H+=NH4+
AD
分析:A、浓硝酸具有强氧化性,反应为Cu+4HNO3═Cu(NO3)2+2NO2↑+2H2O;
B、次氯酸为弱电解质,在离子反应中应保留化学式;
C、没有配平,电荷不守恒、电子不守恒;
D、氨气与盐酸反应生成氯化铵,氨气应保留化学式.
解答:A、将少量铜屑放入浓硝酸中的反应为Cu+4HNO3═Cu(NO3)2+2NO2↑+2H2O,离子反应为Cu+4H++2NO3-=Cu2++2NO2↑+2H2O,故A正确;
B、氯气与水反应为Cl2+H2O=HCl+HClO,离子反应为Cl2+H2O=H++Cl-+HClO,故B错误;
C、向氯化亚铁溶液中通入氯气的反应为2FeCl2+Cl2=2FeCl3,离子反应为2Fe2++Cl2=2Fe3++2Cl-,故C错误;
D、氨气通入盐酸中的反应为NH3+HCl=NH4Cl,其离子反应为NH3+H+=NH4+,故D正确;
故选AD.
点评:本题考查离子反应方程式书写的正误判断,是高考中常考考点,应注意利用电荷守恒及质量守恒定律来分析书写是否正确.
分析:A、浓硝酸具有强氧化性,反应为Cu+4HNO3═Cu(NO3)2+2NO2↑+2H2O;
B、次氯酸为弱电解质,在离子反应中应保留化学式;
C、没有配平,电荷不守恒、电子不守恒;
D、氨气与盐酸反应生成氯化铵,氨气应保留化学式.
解答:A、将少量铜屑放入浓硝酸中的反应为Cu+4HNO3═Cu(NO3)2+2NO2↑+2H2O,离子反应为Cu+4H++2NO3-=Cu2++2NO2↑+2H2O,故A正确;
B、氯气与水反应为Cl2+H2O=HCl+HClO,离子反应为Cl2+H2O=H++Cl-+HClO,故B错误;
C、向氯化亚铁溶液中通入氯气的反应为2FeCl2+Cl2=2FeCl3,离子反应为2Fe2++Cl2=2Fe3++2Cl-,故C错误;
D、氨气通入盐酸中的反应为NH3+HCl=NH4Cl,其离子反应为NH3+H+=NH4+,故D正确;
故选AD.
点评:本题考查离子反应方程式书写的正误判断,是高考中常考考点,应注意利用电荷守恒及质量守恒定律来分析书写是否正确.

练习册系列答案
相关题目
铁及其化合物在生产、生活中有广泛应用。请回答下列问题:
(1)水热法制备Fe3O4纳米颗粒的反应是:3Fe2++2S2O32-+O2+xOH-→Fe3O4↓+S4O32-+2H2O
①上述离子方程式中x=________;
②每生成1 mol Fe3O4,反应转移的电子为________mol;
(2)某高效净水剂可由Fe(OH)SO4聚合得到。工业上以FeSO4、NaNO2和稀硫酸为原料来制备Fe(OH)SO4,反应中有NO生成,化学方程式为 。
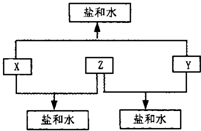
高炉炼铁过程中发生的主要反应为: Fe2O3(s)+ CO(g)
Fe2O3(s)+ CO(g)

 Fe(s)+CO2(g)+Q
Fe(s)+CO2(g)+Q
已知该反应在不同温度下的平衡常数如下:
|
温度/℃ |
1000 |
1115 |
1300 |
|
平衡常数 |
4.0 |
3.7 |
3.5 |
(3)该反应的平衡常数表达式K=_ ;Q 0(填“>”、“<”或“=”);
(4)欲提高上述反应中CO的平衡转化率,可采取的措施是 ;
A.提高反应温度 B.移出部分CO2
C.加入合适的催化剂 D.减小容器的容积
(5)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,此时v正 v逆(填“等于”、“大于”或“小于”)。经过l0 min,在1000℃达到平衡,则该时间范围内反应的平均反应速率v (CO2)= 。



 式 。
式 。