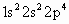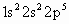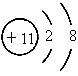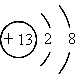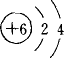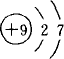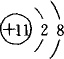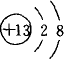题目内容
在下列所表示的微粒中,得电子能力最强的是( )
A、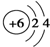 | B、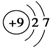 | C、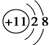 | D、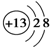 |
分析:非金属性越强,得电子的能力越强,同周期自左而右非金属性增强,同主族自上而下非金属性减弱,据此判断.
解答:解:A和B是分别是碳和氟同周期非金属,得电子能力增强,而CD,分别是钠离子和铝离子较稳定,不再具有氧化性,所以得电子能力最强的是氟,故选B.
点评:本题考查金属元素位置与性质的关系,比较基础,注意理解掌握元素周期律.

练习册系列答案
相关题目
在25℃时,将0.1mol?L-1的HA溶液与0.1mol?L-1的NaOH溶液等体积混合后,测得混合溶液pH=8,则下列所表示的该混合溶液中有关微粒的浓度关系中,错误的是( )
| A、c(HA)+c(A-)=c(Na+)=0.1mol?L-1 | B、c(Na+)-c(A-)=c(OH-)-c(H+) | C、c(Na+)>c(A-)>c(OH-)>c(H+) | D、c(OH-)=c(H+)+c(HA) |