题目内容
18.对可逆反应N2(g)+3H2(g)?2NH3(g)△H<0,下列图象正确( )| A. |  | B. |  | C. |  | D. |  |
分析 A.先拐先平压强大,P1>P2,反应是气体体积减小的反应,压强越大平衡正向进行;
B.反应是放热反应,升温平衡逆向进行;
C.增大氮气浓度平衡正向进行,逆反应速率此时刻不变;
D.催化剂改变反应速率不改变化学平衡,气体压强不变;
解答 解:A.先拐先平压强大,P1>P2,反应是气体体积减小的反应,压强越大平衡正向进行,氨气体积分数应增大,但图象中P1表示的曲线不符合,故A错误;
B.反应是放热反应,升温平衡逆向进行,氮气转化率减小,图象不符合,故B错误;
C.增大氮气浓度平衡正向进行,逆反应速率此时刻不变,随反应正向进行,正反应速率减小,逆反应速率增大,最后达到新的平衡状态,图象不符合,故C正确;
D.催化剂改变反应速率不改变化学平衡,缩短达到平衡的时间,所以混合气体压强不变,图象不符合,故D错误;
故选C.
点评 本题考查了化学平衡影响因素分析,图象的变化特征理解应用,掌握化学平衡移动原理实质和反应特征是解题关键,题目较简单.

练习册系列答案
相关题目
10.已知NA为阿伏伽德罗常数,下列说法中正确的是( )
| A. | 标准状况下,22.4LBr2的物质的量为1mol | |
| B. | 1mol的氯酸钾中氯离子的数目为NA | |
| C. | 87g二氧化锰和足量的热的浓盐酸充分反应,转移的电子数为2NA | |
| D. | 250g的CuSO4•5H2O溶于1L的水,则硫酸铜的浓度为1mol/L |
11.目前出现的元素周期表不少于700种,有平面形、环形、塔形、扇形、台阶形、三角式、透视式、环式、“8”式,等等.这些周期表有的对称美妙,有的奇异专业…下列有关现在的长式周期表的判断中正确的是( )
| A. | 从左往右数第七纵行是第ⅦA族 | |
| B. | 所含元素种类最多的周期是第六周期 | |
| C. | 第IA族的全部元素是金属元素 | |
| D. | 第ⅥA族的全部元素只能表现出非金属的性质 |
6.强酸性溶液X中可能含有Na+、K+、NH4+、Fe2+、A13+、CO32-、SO32-、SO42-、C1-中的若干种,某同学为了确认其成分,取X溶液进行连续实验,实验过程及产物如下:

下列结论正确的是( )

下列结论正确的是( )
| A. | X中肯定存在Na+、Fe2+、A13+、NH4+、SO42- | |
| B. | 气体F在氧气中经催化氧化可生成气体A | |
| C. | 沉淀C一定是BaSO4、沉淀G一定是Fe(OH)3、沉淀I一定是Al(OH )3 | |
| D. | X中不能确定的离子是Fe2+、SO32-、K+和C1- |
13.下列有关化学平衡和速率的说法正确的是( )
| A. | H2、I2、HI平衡混合气体加压后颜色不变 | |
| B. | 恒温恒压的密闭体系中进行的合成氨反应,达到平衡后,充入惰性气体,氨气的体积分数增大 | |
| C. | 红棕色的NO2气体加压后,颜色先变深,后变浅 | |
| D. | 任意温度下都能自发的反应一定是放热和熵减的反应 |
3.在一密闭容器中,反应aA(g)?bB(g)达到平衡后,保持温度不变,将容器体积扩大到原体积的2倍,达到新的平衡后,B的浓度是原来的0.6倍,则下列叙述不正确的是( )
| A. | 平衡向正反应方向移动 | B. | 物质A的转化率增大 | ||
| C. | 物质B的质量分数增加 | D. | a>b |
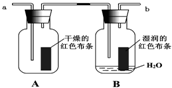 为了探究“红色布条褪色的原因与次氯酸有关而跟氯气无关”.某学生设计了如图装置进行实验.请回答:
为了探究“红色布条褪色的原因与次氯酸有关而跟氯气无关”.某学生设计了如图装置进行实验.请回答:
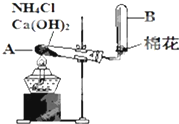 如图是实验室用氯化铵和熟石灰制取氨气的实验装置图.请回答以下各问题:
如图是实验室用氯化铵和熟石灰制取氨气的实验装置图.请回答以下各问题: