题目内容
下列化学用语使用不正确的是( )
A、Na+的结构示意图为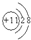 | B、硫酸钠的电离方程式为Na2SO4=2Na++SO42-氯化 | C、乙烯的结构简式为CH2CH2 | D、氯化氢的电子式为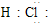 |
分析:A.Na+的质子数为11,核外电子数为10,有2个电子层,最外层电子数为8;
B.先判断电解质的强弱,强电解质用“═”,电离方程式应遵循质量守恒定律和电荷守恒,并注意原子团不可拆分来解答;
C.乙烯的结构简式要体现官能团;
D.氯化氢是共价化合物.
B.先判断电解质的强弱,强电解质用“═”,电离方程式应遵循质量守恒定律和电荷守恒,并注意原子团不可拆分来解答;
C.乙烯的结构简式要体现官能团;
D.氯化氢是共价化合物.
解答:解:A.Na+的质子数为11,核外电子数为10,有2个电子层,最外层电子数为8,结构示意图为 ,故A正确;
,故A正确;
B.Na2SO4为强电解质,电离方程式为Na2SO4=2Na++SO42-,遵循质量守恒定律和电荷守恒,故B正确;
C.乙烯的结构简式必须能体现出其不饱和键,结构简式应为CH2=CH2,故C错误;
D.氯化氢是共价化合物,所以其电子式为: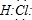 ,故D正确.
,故D正确.
故选C.
 ,故A正确;
,故A正确; B.Na2SO4为强电解质,电离方程式为Na2SO4=2Na++SO42-,遵循质量守恒定律和电荷守恒,故B正确;
C.乙烯的结构简式必须能体现出其不饱和键,结构简式应为CH2=CH2,故C错误;
D.氯化氢是共价化合物,所以其电子式为:
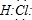 ,故D正确.
,故D正确.故选C.
点评:本题考查原子结构示意图、电离方程式、结构简式和电子式,题目难度不大,注意碳碳双键在结构简式中不能省略.

练习册系列答案
相关题目