题目内容
8.NA表示阿伏加德罗常数的值,下列有关说法正确的是( )| A. | 常温常压下,16g14CH4所含中子数目为8NA | |
| B. | 标准状况下,7.8g苯中含碳碳双键的数目为0.3 NA | |
| C. | 含0.2NA个阴离子的Na2O2和水完全反应转移0.2mol电子 | |
| D. | 0.1L 3mol•L-1的NH4NO3溶液中含有的NH4+数目为0.3N |
分析 A.14CH4的摩尔质量为18g/mol,其分子中含有8个中子;
B.苯分子中不存在碳碳双键;
C.含0.2NA个阴离子的Na2O2的物质的量为0.2mol,0.2mol过氧化钠与水完全反应生成0.1mol氧气,转移了0.2mol电子;
D.铵根离子部分水解,则溶液中铵根离子数目减少.
解答 解:A.16g14CH4的物质的量为:$\frac{16g}{18g/mol}$=$\frac{8}{9}$mol,含中子的物质的量为:$\frac{8}{9}$mol×8=$\frac{64}{9}$mol<8mol,则含有的中子数目小于8NA,故A错误;
B.7.8g苯的物质的量为0.1mol,苯分子中不存在含碳碳双键,故B错误;
C.过氧化钠中的阴离子为过氧根离子,则含0.2NA个阴离子的Na2O2的物质的量为0.2mol,0.2mol过氧化钠与水完全反应生成0.1mol氧气,转移了0.2mol电子,故C正确;
D.0.1L 3mol•L-1的NH4NO3溶液中含有溶质硝酸铵0.3mol,由于铵根离子部分水解,则溶液中含有的NH4+数目小于0.3NA,故D错误;
故选C.
点评 本题考查阿伏加德罗常数的综合应用,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,B为易错点,明确苯分子中不存在碳碳双键为解答关键.

练习册系列答案
相关题目
19.按糖类的现代定义,下列物质不属于糖类的是( )
① ②
②
③ ④
④
①
 ②
②
③
 ④
④
| A. | ②③ | B. | ①④ | C. | ③④ | D. | ②④ |
13.下列溶液中的Cl-的物质的量浓度与100mL 1mol•L-1AlCl3溶液中Cl-的物质的量浓度相等的是( )
| A. | 50mL 3 mol•L-1的KCl溶液 | B. | 150mL 1 mol•L-1的FeCl2溶液 | ||
| C. | 150mL 1 mol•L-1的MgCl2溶液 | D. | 300mL 1 mol•L-1的NaCl溶液 |
20.用下列装置进行的相应实验能达到实验目的是( )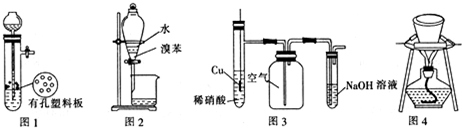

| A. | 图1装置用于Cu和浓H2SO4反应制取少量的SO2气体 | |
| B. | 图2装置用于分离水和溴苯的混合物 | |
| C. | 图3装置用于制备并收集NO气体 | |
| D. | 图4装置用于除去碳酸氢钠固体中的少量碳酸钠 |
17.下列有关物质的性质或应用正确的是( )
| A. | 实验室常用铝盐溶液与氢氧化钠溶液制备Al(OH)3沉淀 | |
| B. | 浓硫酸能干燥SO2、NO2等气体,说明浓硫酸具有吸水性 | |
| C. | SO2 具有漂白性,通入紫色石蕊溶液中能使溶液先变红后褪色 | |
| D. | 30%的H2O2溶液中加入MnO2可制得O2,MnO2做氧化剂 |
18.铝粉投入某无色澄清溶液中产生H2,则该溶液中下列离子组一定可以共存的是( )
| A. | Cl-、SO42-、Mg2+、Al3+ | B. | Na+、K+、Cl-、SO42- | ||
| C. | Na+、K+、Cl-、CO32- | D. | Na+、Fe3+、Cl-、HCO3- |
 有A、B、C、D、E、F六种物质,它们的相互转化关系如图(反应条件及部分产物乙略).已知A、B、E均为单质,B、E在常温下为气体,C为淡黄色固体.回答下列问题:
有A、B、C、D、E、F六种物质,它们的相互转化关系如图(反应条件及部分产物乙略).已知A、B、E均为单质,B、E在常温下为气体,C为淡黄色固体.回答下列问题: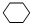 ,名称是环己烷.
,名称是环己烷.