题目内容
下列物质中,属于强电解质的是 ,属于弱电解质 ,属于非电解质的是 .(填序号)
A.氯化钠 B.硫酸溶液 C.醋酸 D.氯化银 E.氨气 F.铜 G.氢氧化铜.
A.氯化钠 B.硫酸溶液 C.醋酸 D.氯化银 E.氨气 F.铜 G.氢氧化铜.
考点:强电解质和弱电解质的概念,电解质与非电解质
专题:电离平衡与溶液的pH专题
分析:电解质是指:在水溶液中或熔融状态下能够导电的化合物;电解质水溶液中或熔融状态下能够导电,是因电解质自身可以离解成自由移动的离子;
强电解质是在水溶液中或熔融状态下能完全电离的电解质,包括强酸、强碱、活泼金属氧化物和大部分盐;
弱电解质是指:在水溶液里部分电离的电解质,包括弱酸、弱碱、水与少数盐;
非电解质是指:在水溶液里和熔融状态下都不导电的化合物;
单质、混合物,既不是电解质也不是非电解质,据此分析即可解答.
强电解质是在水溶液中或熔融状态下能完全电离的电解质,包括强酸、强碱、活泼金属氧化物和大部分盐;
弱电解质是指:在水溶液里部分电离的电解质,包括弱酸、弱碱、水与少数盐;
非电解质是指:在水溶液里和熔融状态下都不导电的化合物;
单质、混合物,既不是电解质也不是非电解质,据此分析即可解答.
解答:
解:根据电解质、非电解质、强电解质和弱电解质的概念分析;强、弱电解质的区别在于其在水溶液中能否完全电离,电解质和非电解质都指的是化合物.
氨气(NH3)本身不电离,又是化合物,所以是非电解质;
铜是单质,既不是电解质也不是非电解质;
硫酸溶液是混合物,即不是电解质也不是非电解质;
“酸、碱、盐、水都是电解质”,所以氯化钠、醋酸、氯化银、氢氧化铜都是电解质,强电解质包括强酸、强碱和绝大多数盐,所以氯化钠和氯化银为强电解质,
弱电解质包括弱酸、弱碱、极少数盐和水,所以醋酸和氢氧化铜为弱电解质;
故答案为:A D; C G; E.
氨气(NH3)本身不电离,又是化合物,所以是非电解质;
铜是单质,既不是电解质也不是非电解质;
硫酸溶液是混合物,即不是电解质也不是非电解质;
“酸、碱、盐、水都是电解质”,所以氯化钠、醋酸、氯化银、氢氧化铜都是电解质,强电解质包括强酸、强碱和绝大多数盐,所以氯化钠和氯化银为强电解质,
弱电解质包括弱酸、弱碱、极少数盐和水,所以醋酸和氢氧化铜为弱电解质;
故答案为:A D; C G; E.
点评:本题考查了电解质、非电解质、强电解质、弱电解质的判断,题目难度不大,注意电解质的强弱与电离程度有关与溶液的导电能力无关.

练习册系列答案
相关题目
将溴水中的溴萃取出来的实验中,下列说法错误的是( )
| A、分液漏斗使用前要检验它是否漏水 |
| B、可以选用酒精作为萃取剂 |
| C、溴在萃取剂中的溶解度要大于在水的溶解度 |
| D、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
难挥发性二硫化钽(TaS2)可采用如图装置提纯.将不纯的TaS2粉末装入石英管一端,抽真空后加入适量碘并封管,置于加热炉中,发生反应:TaS2(s)+2I2(g)
TaI4(g)+S2(g).下列说法正确的是( )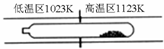
| 1123K |
| 1023K |

| A、在不同温度区域,TaI4的量保持不变 |
| B、在提纯过程中,I2的量不断减少 |
| C、该反应的平衡常数与TaI4和S2的浓度乘积成反比 |
| D、在提纯过程中,I2的作用是将TaS2从高温区转移到低温区 |
下列物质属于电解质并能导电的是( )
①熔融的NaCl ②KNO3溶液 ③Cu ④酒精 ⑤KCl晶体.
①熔融的NaCl ②KNO3溶液 ③Cu ④酒精 ⑤KCl晶体.
| A、① | B、①② |
| C、①②⑤ | D、①②③⑤ |
下列说法中正确的是(NA表示阿伏加德罗常数)( )
| A、0.1 mol H2O中所含的原子总数是0.3NA |
| B、在常温常压下,11.2L氯气所含的原子数为NA |
| C、标准状况下,22.4L氢气所含的质子数为2 2.4NA |
| D、2L 1mol?L-1K2SO4溶液中离子的总数为3 NA |
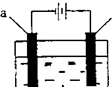 下列对如图所示装置实验现象的描述正确的是( )
下列对如图所示装置实验现象的描述正确的是( )