题目内容
Ⅰ(11分).已知25℃时CH3COOH和NH3?H2O的电离程度相同。现有常温下1 mol/L的醋酸溶液和1 mol/L的氨水,且知醋酸溶液的pH=a,试回答下列问题:
(1)醋酸溶液中存在的电离平衡用电离方程式表示为: ,在同样条件下,该浓度的氨水的pH= (用含a的代数式表达)。
(2)将上述两种溶液等体积混合,所得溶液的pH=___________。
(3)饱和氯化铵溶液显 性,原因是
。
Ⅱ.(8分)已知在0.1 mol?L-1的NaHSO3溶液中有关微粒浓度由大到小的顺序为:
c(Na+)>c(HSO3-)>c(SO32-)>c(H2SO3),则该溶液中,c(H+) c(OH-)(填“>”、“<”或“=”),简述理由并写出相关的方程式
。
Ⅰ、⑴;CH3COOH![]() CH3COO- +H+ ,14-a⑵7
CH3COO- +H+ ,14-a⑵7
⑶酸性;NH4+ + H2O ![]() NH3 ?H2O + H+ 因NH4+水解,使得c(H+)>c(OH-),溶液显酸性.
NH3 ?H2O + H+ 因NH4+水解,使得c(H+)>c(OH-),溶液显酸性.
Ⅱ、〉;亚硫酸氢根离子电离显酸性:HSO3-![]() H++SO32-,亚硫酸氢根离子水解 显碱性:HSO3-+H2O
H++SO32-,亚硫酸氢根离子水解 显碱性:HSO3-+H2O![]() H2SO3+OH-电离程度大于水解,溶液显酸性。
H2SO3+OH-电离程度大于水解,溶液显酸性。


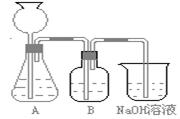
 (5)实验室制取下列气体:①NH3,②Cl2,③HCl,④H2S,⑤CH4,⑥CO,⑦CO2,⑧O2时,属于必须进行尾气处理,并能用下图所示装置进行处理的,将气体的序号填入装置图的下方空格内。
(5)实验室制取下列气体:①NH3,②Cl2,③HCl,④H2S,⑤CH4,⑥CO,⑦CO2,⑧O2时,属于必须进行尾气处理,并能用下图所示装置进行处理的,将气体的序号填入装置图的下方空格内。
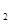 O外,还有H
O外,还有H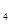 外,还有C
外,还有C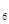 等;与之相似的氮元素的氢化物除外,还有N
等;与之相似的氮元素的氢化物除外,还有N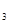 对农业、化学、国防工业具有重要意义。其合成原理为:
对农业、化学、国防工业具有重要意义。其合成原理为: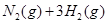

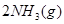
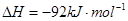
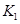 =
(只列数字表达式)
=
(只列数字表达式)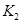 ,同
,同