题目内容
(12分)某研究性学习小组探究在含有盐酸的Cu2+、Ca2+的混合溶液中滴加Na2CO3溶液时发生反应的过程。(已知 Ksp{Cu(OH)2小于Ksp(CuCO3)}
取适量样品溶液,插入pH传感器并逐滴滴入Na2CO3溶液,测得pH变化曲线如下图所示:
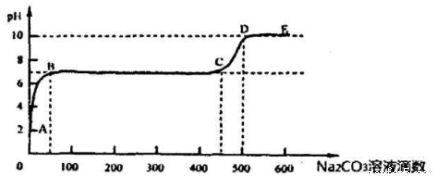
(1)为简单而精确地控制加入的Na2CO3溶液的体积,可将碳酸钠溶液置于 (填仪器名称)中滴加。
(2)图中有二个pH增加较快的阶段,第一阶段(a点前)对应的实验现象是 。
(3)对于a.b之间溶液PH值变化缓慢的本质,该小组同学做出了如下推测,请补充推测2和3:
推测1:生成了Cu(OH)2沉淀,消耗了CO32-;推测2: ;
推测3: ;
若推测1符合实际情况,则此情况下反应的离子方程式为 ;
(4)请设计实验验证检测推测1,不要写出详细的实验过程,试剂不受限制。
实验方法、步骤 | 实验现象和结论 |
|
|
(1)碱式滴定管(2分);(2)有无色无味的气体产生(2分);
(3)推测2:生成了CaCO3沉淀,消耗了CO32-(1分)
推测3:既生成了CaCO3沉淀,又生成了Cu(OH)2沉淀,都消耗了CO32-;(1分)
CO32-+Cu2++H2O== Cu(OH)2↓+CO2↑(2分)
(4)
实验方法、步骤 | 实验现象和结论 |
取适量洗涤、干燥后的沉淀充分加热,将产生的气体依次通过无水硫酸铜、澄清石灰水。(2分) (每步1分,共2分) | 若加热时蓝色固体变为黑色,无水硫酸铜由白变蓝,澄清石灰水不变浑浊,则推测1成立,否则不成立。(2分) (每个现象1分,共2分) |
【解析】
试题分析:(1)Na2CO3是强碱弱酸盐,水溶液显碱性,所以为简单而精确地控制加入的Na2CO3溶液的体积,可将碳酸钠溶液置于碱式滴定管中滴加;(2)图中有二个pH增加较快的阶段,第一阶段(a点前)发生的反应是HCl和Na2CO3反应产生气体,所以对应的实验现象是有无色无味的气体产生;(3)推测1:生成了Cu(OH)2沉淀,消耗了CO32-;推测2:生成了CaCO3沉淀,消耗了CO32-;推测3:既生成了CaCO3沉淀,又生成了Cu(OH)2沉淀,都消耗了CO32-;若推测1符合实际情况,根据电荷守恒及原子守恒可知,在此情况下反应的离子方程式为:CO32-+Cu2++H2O== Cu(OH)2↓+CO2↑; (4)验证检测推测1是实验操作是取适量洗涤、干燥后的沉淀充分加热,将产生的气体依次通过无水硫酸铜、澄清石灰水。若会观察到:加热时蓝色固体变为黑色,无水硫酸铜由白色变为蓝色,澄清石灰水不变浑浊,则推测1成立,否则不成立。
考点:考查物质成分的确定、实验方案是设计、与检验、离子方程式的书写的知识。

用如图所示装置制取表格中的四种干燥、纯净的气体(必要时可以加热;a、b、c、d表示相应仪器中加入的试剂)。其中正确的是

选项 | 气体 | a | b | c | d |
A | SO2 | 浓硫酸 | Cu | H2O | 浓硫酸 |
B | Cl2 | 浓盐酸 | MnO2 | NaOH溶液 | 浓硫酸 |
C | NH3 | 饱和NH4Cl溶液 | 消石灰 | 空集气瓶 | 固体NaOH |
D | NO | 稀硝酸 | 铜屑 | H2O | 浓硫酸 |