��Ŀ����
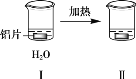
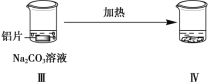
����Ŀ��̽����Ƭ��Na2CO3��Һ�ķ�Ӧ��
|
| |
���������� | ��Ƭ�������ϸС���� | ���ְ�ɫ���ǣ������������ݣ�������ΪH2��CO2�� |
����˵������ȷ����
A.�ԱȢ�˵��Na2CO3��Һ���ƻ�������ı���Ĥ
B.�Ʋ���ְ�ɫ���ǵ�ԭ��AlO2- + HCO3- + H2O = Al��OH��3��+ CO32-
C.���Ⱥ�H2�ݳ���CO32- ˮ��ƽ���ƶ������Ӱ�����෴��
D.Na2CO3��Һ�д���ˮ��ƽ�⣺CO32- + H2O HCO3- + OH-
���𰸡�C
��������
Aѡ�I��Al����û�����ݣ�˵������������Ĥ��III��Al�����ݣ�˵����������Ĥ���ƻ�����A��ȷ��
Bѡ�̼������Һ�Լ��ԣ������������Ĥ�ͼӦ����ƫ�������ȥ������Ĥ�����ͼӦ����ƫ�������̼���ˮ������̼�������̼��������Ӻ�ƫ��������ӷ�Ӧ�� AlO2�� + HCO3�� + H2O = Al(OH)3��+ CO32������B��ȷ��
Cѡ�����ˮ�������ȷ�Ӧ�����ȴٽ�����ˮ�⣬�����ݳ��������������������ӵķ�Ӧ��̼���ˮ������̼����������������ӣ����������������ӣ��ٽ�̼�������ˮ�⣬���Լ��Ⱥ�H2�ݳ���CO32- ˮ��ƽ���ƶ������ٽ����ã���C����
Dѡ�Na2CO3��Һ�д���ˮ��ƽ�⣺CO32�� + H2O ![]() HCO3�� + OH������D��ȷ��
HCO3�� + OH������D��ȷ��
������������ΪC��