��Ŀ����
���ܱ������У���1.0molCO��1.0molH2O��ϼ��ȵ�800�棬�������з�Ӧ��
CO(g)+H2O(g) CO2(g)+H2(g)��һ��ʱ���÷�Ӧ�ﵽƽ�⣬���CO�����ʵ���Ϊ0.5mol����
CO2(g)+H2(g)��һ��ʱ���÷�Ӧ�ﵽƽ�⣬���CO�����ʵ���Ϊ0.5mol����
(1)�ﵽƽ��ʱCO2�����ʵ��������÷�Ӧ�Ļ�ѧƽ�ⳣ����
(2)�ﵽƽ������ƽ����ϵ��ͨ��1.0molˮ�������ﵽ�µ�ƽ��״̬ʱ����ˮ���������ʵ�����CO2�����ʵ���������
CO(g)+H2O(g)
 CO2(g)+H2(g)��һ��ʱ���÷�Ӧ�ﵽƽ�⣬���CO�����ʵ���Ϊ0.5mol����
CO2(g)+H2(g)��һ��ʱ���÷�Ӧ�ﵽƽ�⣬���CO�����ʵ���Ϊ0.5mol����(1)�ﵽƽ��ʱCO2�����ʵ��������÷�Ӧ�Ļ�ѧƽ�ⳣ����
(2)�ﵽƽ������ƽ����ϵ��ͨ��1.0molˮ�������ﵽ�µ�ƽ��״̬ʱ����ˮ���������ʵ�����CO2�����ʵ���������
(1)25% 1
(2)1.33mol 22.22%
(2)1.33mol 22.22%
��������� CO(g) + H2O(g)
 CO2(g) + H2(g)
CO2(g) + H2(g)��ʼ���ʵ����� 1.0mol 1.0mol 0 0
ת���� x x x x
ƽ�����ʵ����� (1-x)mol (1-x)mol x x
�������֪�� x=0.5mol
�ﵽƽ��ʱCO2�����ʵ�������Ϊ��x/2=0.25=25%
�÷�Ӧ�Ļ�ѧƽ�ⳣ��:

�� CO(g) + H2O(g)
 CO2(g) + H2(g)
CO2(g) + H2(g)ƽ��ʱ�����ʵ�Ũ�ȣ� 0.5mol 0.5mol 0.5mol 0.5mol
ͨ��1.0molˮ������ 0.5mol 1.5mol 0.5mol 0.5mol
ת���� y y y y
�ٴ�ƽ�⣺ ��0.5-y�� (1.5-y) (0.5+y) (0.5+y)
����ƽ�ⳣ���У�

��֮�ã�

ˮ���������ʵ���:n(H2O)=1.5-0.5/3=4/3mol
CO2�����ʵ�������:


��ϰ��ϵ�д�
 �Ƹ�С״Ԫͬ������������ϵ�д�
�Ƹ�С״Ԫͬ������������ϵ�д�
�����Ŀ
 2AB3(g)��ѧƽ��״̬��Ӱ�죬�õ�����ͼ��ʾ�ı仯���ɣ�T��ʾ�¶ȣ������н�����ȷ����
2AB3(g)��ѧƽ��״̬��Ӱ�죬�õ�����ͼ��ʾ�ı仯���ɣ�T��ʾ�¶ȣ������н�����ȷ����
 2Z(g)����H��0���ﵽƽ��ʱ������˵����ȷ���ǣ�
2Z(g)����H��0���ﵽƽ��ʱ������˵����ȷ���ǣ�
 2C(��) ��H ��0����ƽ������������г��� amolC(g),�ٴ�ƽ�����ԭƽ��Ƚϣ�����������ȷ����
2C(��) ��H ��0����ƽ������������г��� amolC(g),�ٴ�ƽ�����ԭƽ��Ƚϣ�����������ȷ���� 3C(g)+D(g)���ﵽƽ��ʱ��C��Ũ��ΪW mol/L����ά������������¶Ȳ��䣬���������ַ����ı���ʼ���ʣ��ﵽƽ���C��Ũ����ΪWmol/L����
3C(g)+D(g)���ﵽƽ��ʱ��C��Ũ��ΪW mol/L����ά������������¶Ȳ��䣬���������ַ����ı���ʼ���ʣ��ﵽƽ���C��Ũ����ΪWmol/L����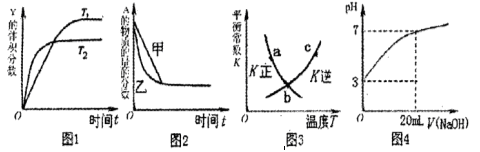
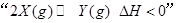 �¶�
�¶�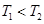 ������
������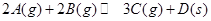 ��Ӱ�죬�ҵ�ѹǿ�ȼ�ѹǿ��
��Ӱ�죬�ҵ�ѹǿ�ȼ�ѹǿ�� 3FcS(s)+4H2O(g) ��H=a kJ ? mol-1
3FcS(s)+4H2O(g) ��H=a kJ ? mol-1