题目内容
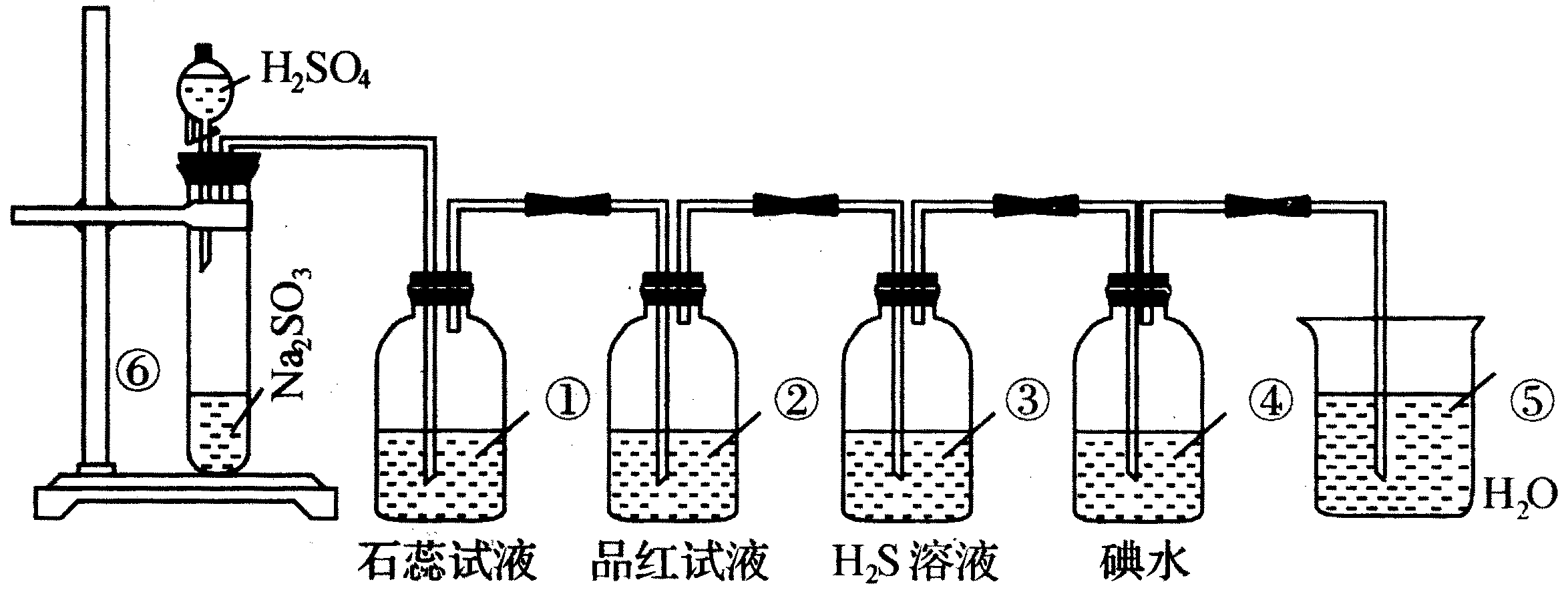
图所示是实验室制取SO2并验证SO2的某些性质的装置图.试回答:
(1)在⑥中发生的化学反应方程式为________.
(2)①中的实验现象为________,此实验证明SO2是________气体.
(3)②中的品红溶液________,证明SO2有________.
(4)③中的实验现象是________,证明SO2有________性.
(5)④中的实验现象是________,证明SO2有________性.
(6)⑤的作用是________,反应的化学方程式为________.
答案:
解析:
解析:
|
(1)Na2SO3+H2SO4=Na2SO4+SO2↑+H2O (2)石蕊试液变红,酸性. (3)褪色,漂白性. (4)变浑浊,氧化. (5)褪色,还原. (6)吸收多余的SO2,防止污染空气,SO2+H2O=H2SO3 |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
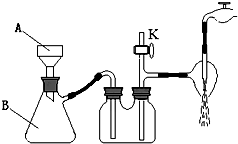 高氯酸钾广泛用于火箭及热电池业.实验室制取高氯酸钾的原理与苏教版《实验化学》中“硝酸钾晶体的制备”相同,步骤为:称取一定质量的KCl、NaClO4加热溶解,经冷却结晶、过滤、滤出晶体用蒸馏水多次洗涤及真空干燥得到.
高氯酸钾广泛用于火箭及热电池业.实验室制取高氯酸钾的原理与苏教版《实验化学》中“硝酸钾晶体的制备”相同,步骤为:称取一定质量的KCl、NaClO4加热溶解,经冷却结晶、过滤、滤出晶体用蒸馏水多次洗涤及真空干燥得到.




