题目内容
在标准状况下,11.2LA2气体和33.6LB2气体刚好完全反应,合成22.4LC气体,则C气体的化学式是:________;经测定该A2气体质量是14g,B2气体质量是3g,求C气体的摩尔质量是:________.
AB3 17g/mol
分析:根据阿伏加德罗定律和质量守恒定律判断化学式,根据M=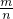 计算C气体的摩尔质量.
计算C气体的摩尔质量.
解答:在相同条件下,气体的体积之比等于气体的物质的量之比,则
n(A2):n(B2):n(C)=11.2:33.6:22.4=1:3:2,则有:
A2+3B2=2C,
反应前后气体的质量不变,则C的化学式为AB3,
n(C)=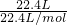 =1mol,
=1mol,
m(C)=m(A2)+m(B2)=14g+3g=17g,
所以:M(C)=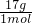 =17g/mol,
=17g/mol,
故答案为:AB3;17g/mol.
点评:本题考查物质化学式和气体摩尔质量的计算,题目难度不大,注意阿伏加德罗定律和质量守恒定律的应用.
分析:根据阿伏加德罗定律和质量守恒定律判断化学式,根据M=
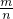 计算C气体的摩尔质量.
计算C气体的摩尔质量.解答:在相同条件下,气体的体积之比等于气体的物质的量之比,则
n(A2):n(B2):n(C)=11.2:33.6:22.4=1:3:2,则有:
A2+3B2=2C,
反应前后气体的质量不变,则C的化学式为AB3,
n(C)=
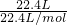 =1mol,
=1mol,m(C)=m(A2)+m(B2)=14g+3g=17g,
所以:M(C)=
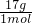 =17g/mol,
=17g/mol,故答案为:AB3;17g/mol.
点评:本题考查物质化学式和气体摩尔质量的计算,题目难度不大,注意阿伏加德罗定律和质量守恒定律的应用.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目