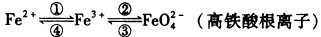��Ŀ����
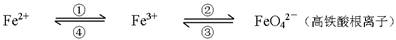
�����仯����֮����ת��������ʽ��ʾ��
|
|
![]()
![]() Fe2+ Fe3+ FeO42-
Fe2+ Fe3+ FeO42-
�ش������й����⣺
��1��Fe�����ϡ���ᷴӦ������ȡFeSO4�����÷�Ӧ���õ�������Һʵ�������ٵ�ת����Ҫ����﴿������ѡ�õ��Լ��� ��ѡ����ţ���
a��Cl2 b��Fe c��HNO3 d��H2O2
��2������ת���õ��������������ڵ绯������ͭ���ա����������������ķ�Ӧ�Ƚϸ��ӣ�������һ��Ҫ��Ӧ��CuFeS2+4Fe3+===Cu2++5Fe2++2S��CuFeS2��SΪ-2�ۣ���
������˵����ȷ���� ��ѡ����ţ���
a�������ʵ������������ͭ�����ںϽ�
b����Ӧ�У�������Ԫ�ؾ�����ԭ
c����Ӧ�У�CuFeS2����������������ԭ��
d����ת��1 mol e- ʱ����46 g CuFeS2�μӷ�Ӧ
��3�����������һ�����͡���Ч����ɫ��ˮ�����侻ˮԭ���� ��
��1��d��2�֣� ��2��d��2�֣�
��3��������ؾ���ǿ�����ԣ�����ɱ����������1�֣���ͬʱ���ɵ�Fe3+����ת��Ϊ
Fe��OH��3���壬�ܼ�������������������ã�1�֣���

 �����仯����֮����ת��������ʽ��ʾ���٢ڢۢ�
�����仯����֮����ת��������ʽ��ʾ���٢ڢۢ�