题目内容
Q、W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,Q、W、Z是非金属元素。五种元素核电荷数之和为55,对应原子最外层电子数之和为21。W、Z最外层电子数相同,但Z的核电荷数是W的2倍。
(1)Q在周期表中位于第 周期 族。
(2)X、Y各自的最高价氧化物对应的水化物可以发生反应生成盐和水,请写出该反应的离子方程式: 。
(3)X单质能在W单质中燃烧可生成化合物R,R的电子式 ,该物质所含有的化学键的类型为 。
(4)Z的氢化物与W的氢化物发生反应生成Z单质和水,写出其化学方程式 。
(10分)(1) 二 ⅴA (各1分)(2)Al(OH)3 + OH-= AlO2-+ 2H2O (2分)
(3)  (2分) 离子键,非极性键(答共价键也给分)(2分)
(2分) 离子键,非极性键(答共价键也给分)(2分)
(4)H2S + H2O2 = S↓+ 2H2O (2分)
解析试题分析:W、Z最外层电子数相同,但Z的核电荷数是W的2倍,则符合条件是O和S,所以W是氧元素,Z是硫元素。五种元素核电荷数之和为55,对应原子最外层电子数之和为21。这说明Q、X、Y的核电荷数之和是31,原子最外层电子数之和为9。又因为X、Y是金属元素,Q、W、Z是非金属元素。则根据原子序数经讨论可知,Q应该是氮元素,X是Na元素,Y是铝元素。
考点:考查元素周期表的结构和元素周期律的应用
点评:该题以“周期表中元素的推断”为载体,比较全面考查学生有关元素推断知识和灵活运用知识的能力。考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。

| A、氢化物稳定性:Z>W | B、原子半径的大小顺序:rX>rY>rQ>rW | C、元素Q和Z能形成QZ2型的共价化合物 | D、X、Y的最高价氧化物的水化物之间不能发生反应 |
 Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大,Q是周期表中原子半径最小的元素,Q与W组成的化合物是一种温室气体,W与Y、X与Y组成的化合物是机动车排出的大气污染物,Y和Z能形成原子个数比为1:1和1:2的两种离子化合物.
Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大,Q是周期表中原子半径最小的元素,Q与W组成的化合物是一种温室气体,W与Y、X与Y组成的化合物是机动车排出的大气污染物,Y和Z能形成原子个数比为1:1和1:2的两种离子化合物.
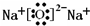
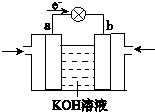
 Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大;W与Q按1:4形成的化合物A是一种重要能源;W与Y,X与Y组成的化合物是常见的大气污染物;Y与Z按1:1形成的离子化合物B,其摩尔质量为78g?mol-1.请回答下列问题.
Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大;W与Q按1:4形成的化合物A是一种重要能源;W与Y,X与Y组成的化合物是常见的大气污染物;Y与Z按1:1形成的离子化合物B,其摩尔质量为78g?mol-1.请回答下列问题.