题目内容
关于浓度相等的三种溶液:①H2CO3 ②NaOH ③Na2CO3溶液,下列说法正确的是( )
| A、水电离出的c(H+):③>①>② |
| B、溶液的pH:③>②>① |
| C、①和②等体积混合后的溶液:c(Na+)=c(H2CO3)+c(HCO3-)+c(CO32-) |
| D、①和③等体积混合后的溶液:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) |
考点:离子浓度大小的比较
专题:电离平衡与溶液的pH专题,盐类的水解专题
分析:A.酸或碱抑制水电离、含有弱离子的盐促进水电离,酸中氢离子浓度或碱中氢氧根离子浓度越大,其抑制水电离程度越大;
B.相同浓度的这几种溶液中,根据溶液的酸碱性判断溶液的pH大小;
C.等物质的量的碳酸和氢氧化钠溶液混合得到碳酸氢钠溶液,根据物料守恒判断;
D.①和③等体积混合,根据混合液中电荷守恒进行判断.
B.相同浓度的这几种溶液中,根据溶液的酸碱性判断溶液的pH大小;
C.等物质的量的碳酸和氢氧化钠溶液混合得到碳酸氢钠溶液,根据物料守恒判断;
D.①和③等体积混合,根据混合液中电荷守恒进行判断.
解答:
解:A.酸或碱抑制水电离、含有弱离子的盐促进水电离,酸中氢离子浓度或碱中氢氧根离子浓度越大,其抑制水电离程度越大,等浓度的这几种溶液,①②抑制水电离、③促进水电离,②中c(OH-)大于①中c(H+),所以NaOH抑制水电离程度大于碳酸,则这几种溶液中水电离出的c(H+):③>①>②,故A正确;
B.碳酸为酸,其溶液呈酸性,氢氧化钠是强碱,其溶液呈强碱性,碳酸钠是强碱弱酸盐,其溶液呈弱碱性,所以等浓度的这几种溶液中pH:②>③>①,故B错误;
C.等物质的量的①和②溶液混合,反应后混合液的溶质为碳酸氢钠,根据物料守恒得:c(Na+)=c(H2CO3)+c(HCO3-)+c(CO32-),故C正确;
D.①和③等体积混合,混合液中一定满足电荷守恒,碳酸根离子带有2个单位负电荷,其系数错误,正确的电荷守恒为:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-),故D错误;
故选AC.
B.碳酸为酸,其溶液呈酸性,氢氧化钠是强碱,其溶液呈强碱性,碳酸钠是强碱弱酸盐,其溶液呈弱碱性,所以等浓度的这几种溶液中pH:②>③>①,故B错误;
C.等物质的量的①和②溶液混合,反应后混合液的溶质为碳酸氢钠,根据物料守恒得:c(Na+)=c(H2CO3)+c(HCO3-)+c(CO32-),故C正确;
D.①和③等体积混合,混合液中一定满足电荷守恒,碳酸根离子带有2个单位负电荷,其系数错误,正确的电荷守恒为:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-),故D错误;
故选AC.
点评:本题考查了离子浓度大小比较,题目难度中等,根据弱电解质的电离、盐类水解等知识点来分析解答,注意守恒思想的灵活运用,试题有利于提高学生的分析、理解能力.

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
 铅蓄电池是典型的可充电型电池,它的正负极格板是惰性材料,电池总反应式为:
铅蓄电池是典型的可充电型电池,它的正负极格板是惰性材料,电池总反应式为:Pb+PbO2+4H++2SO42-
| 放电 |
| 充电 |
| A、放电时:电解液中H2SO4的浓度将变小;正极的电极反应式是PbO2+2e-+4H++SO42-=PbSO4+2H2O |
| B、当外电路通过1mol电子时,理论上负极板的质量增加48g,正极板的质量增加32g |
| C、电池在完全放电耗尽PbO2和Pb时,若按图连接,电解一段时间后,则在A电极上生成PbO2、B电极上生成Pb |
| D、若按图连接,电解一段时间后,此时铅蓄电池的电极的极性将对换 |
化学与社会、环境、生活密切相关.下列说法正确的是( )
| A、食盐、食醋和味精是常用的食品添加剂,其主学成分均属钠盐 |
| B、SO2、C02、NO2均被列入我国空气质量报告的指标 |
| C、青铜是我国使用最早的合金 |
| D、家用84消毒液可用来漂白衣物,为了增强其漂白效果,使用时可加浓盐酸 |
下列有关说法正确的是( )
| A、一定条件下,使用催化剂能加快反应速率但不能改变平衡转化率 |
| B、氢氧燃料电池的能量转换形式仅为化学能转化为电能 |
| C、升高温度水的离子积常数减小 |
| D、根据能量守恒定律,反应物的总能量一定等于生成物的总能量 |
 五种短周期元素(用字母表示)在周期表中的相对位置如图,其中Y的单质在空气中含量最高.下列判断正确的是( )
五种短周期元素(用字母表示)在周期表中的相对位置如图,其中Y的单质在空气中含量最高.下列判断正确的是( )| A、最高价氧化物的水化物的酸性:X>Y |
| B、气态氢化物稳定性:Y<M |
| C、R的氧化物的水化物是离子化合物 |
| D、Z、M、R的原子半径依次减小,最高化合价依次升高 |
通常人们把拆开1mol某化学键所消耗的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H),化学反应的△H等于反应物的总键能与生成物的总键能之差.
工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)
Si(s)+4HCl(g),该反应的反应热△H为( )
| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| 键能/kJ?mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
| ||
| A、+412kJ?mol-1 |
| B、-412kJ?mol-1 |
| C、+236kJ?mol-1 |
| D、-236kJ?mol-1 |
“细节决定成败”对于下列实验细节处理正确的是( )
| A、实验室制氢气:为了加快反应速率,向稀H2SO4滴加少量CuSO4溶液 |
| B、钠与水的反应:取绿豆大小的金属钠放入烧杯,再滴入两滴酚酞试液,最后加入水 |
| C、配置0.10mol/L NaOH溶液:称取0.4g NaOH放入100mL容量瓶,加水至100mL |
| D、配置FeCl2溶液:称取一定量的FeCl2固体,加水溶解,在加入稀盐酸酸化 |
下列说法不正确的是( )
A、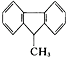 分子中的所有碳原子不可能同时在一个平面内 分子中的所有碳原子不可能同时在一个平面内 |
B、按系统命名法,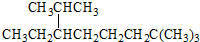 的名称为2,2,7-三甲基-6-乙基辛烷 的名称为2,2,7-三甲基-6-乙基辛烷 |
C、目前市场上大量矿泉水、食用油等产品包装瓶几乎都是用PET(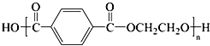 )的合成单体之一是对苯二甲酸 )的合成单体之一是对苯二甲酸 |
| D、有一种信息素的结构简式为CH3(CH2)5CH═CH(CH2)9CHO,为验证该物质中既含有醛基又含有碳碳双键,向该物质的试液中先加过量的溴水溶液,观察到溶液褪色,再向溶液中加入新制的Cu(OH)2悬浊液,加热煮沸,观察到砖红色沉淀 |
某同学将一小块金属钠投入到硫酸铜溶液中,通过此实验不能证明下列性质中的( )
| A、钠比水轻但比煤油重 |
| B、钠的熔点较低 |
| C、钠与水反应时要放出热量 |
| D、钠与水反应后溶液呈碱性 |