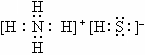题目内容
已知五种元素的原子序数的大小顺序为C>A>B>D>E;A,C同周期;B,C同主族;A与B形成的离子化合物A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10个电子的分子.试回答下列问题:
(1)写出五种元素的符号:
A________,B________,C________,D________,E________.
(2)用电子式表示离子化合物A2B的形成过程________.
(3)写出下列物质的电子式:
①D元素形成的单质________;
②E与C形成的化合物________;
③A,B,E形成的化合物________;
④D,E形成的化合物________;
⑤D,C,E形成的离子化合物________.
答案:
解析:
提示:
解析:
|
【解答】(1)Na,O,S,N,H (2) (3)① 【巧解导析】①因A,B离子的电子数相同,在A2B中电子总数为30,可知每个离子的电子数为10,故A为Na,B为O.②又因4个原子核、10个电子形成的分子中,每个原子平均不到3个电子,所以只好从原子序数为1~8的元素中寻找.Li已有3个电子,可知一定含有氢原子,分子中有4个原子核共10个电子,一定是NH3.因为原子序数D>E,故D为N,E为H.③C与A(Na)同周期,与B(O)同主族,故C位于第三周期ⅥA族,为S. |
提示:
|
【巧解点悟】解题的关键是能够利用原子结构及元素周期表的知识推断出元素,并且能够正确地书写物质的电子式.否则很难将本题全部做对. |

练习册系列答案
相关题目
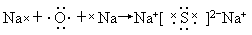
 ;②
;②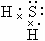 ;③
;③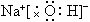 ;④
;④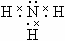 ;⑤
;⑤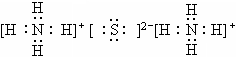 或
或