题目内容
(14分)2SO2(g)+O2(g)  2SO3(g)反应过程的能量变化如图所示。、
2SO3(g)反应过程的能量变化如图所示。、
已知1mol SO2(g)氧化为1mol SO3的ΔH= -99kJ·mol—1.请回答下列问题:(1)图中A、C分别表示 、
,E的大小对该反应的反应热有无影响? 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? ,并说明理由 ;
(2)图中△H= ;
(3)如果反应速率v(SO2)为0.05 mol·L—1·min—1,则v(O2)= mol·L—1·min—1
(4)已知单质硫的燃烧热为296 KJ·mol—1,计算由S(s)生成3 molSO3(g)的△H (要有计算过程)。
(1)反应物能量(1分)、生成物能量(1分) 无(1分)
降低(1分), 因为催化剂改变了反应的历程使活化能E降低 (2分)
(2)—198 KJ·mol—1 (2分)
(3)0.025 (2分)
(4)S(s) + O2(g) = 2SO2(g) △H1=" —" 296 KJ·mol—1,
SO2(g)+1/2O2(g)  SO3(g) △H2=" —99" KJ·mol—1
SO3(g) △H2=" —99" KJ·mol—1
3S(s)+9/2O2(g)=3SO3(g) △H=3(△H1+△H2)=" —1185" KJ·mol—1 (共4分)
解析

练习册系列答案
相关题目
 2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol的ΔH=—99kJ·mol—1.请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol的ΔH=—99kJ·mol—1.请回答下列问题:
 CO(g)+3H2(g) ⊿H1="+206.1" kJ/mol
CO(g)+3H2(g) ⊿H1="+206.1" kJ/mol 的物质的量浓度随反应时间的变化如图1所示。10min时,改变的外界条件可能是 。
的物质的量浓度随反应时间的变化如图1所示。10min时,改变的外界条件可能是 。
 ,使甲、乙两容器初始容积相等。在相同温度下发生反应②,并维持反应过程中温度不变。已知甲容器中
,使甲、乙两容器初始容积相等。在相同温度下发生反应②,并维持反应过程中温度不变。已知甲容器中
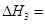 。800℃时,反应③的化学平衡常数K=1.0,某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
。800℃时,反应③的化学平衡常数K=1.0,某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
 (正)
(正) (逆) b.
(逆) b. 2SO3(g);△H=-96.56 kJ?mol-1,甲容器在反应过程中保持压强不变,乙容器保持体积不变,丙容器维持绝热,三容器各自建立化学平衡。
2SO3(g);△H=-96.56 kJ?mol-1,甲容器在反应过程中保持压强不变,乙容器保持体积不变,丙容器维持绝热,三容器各自建立化学平衡。