题目内容
X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种元素为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9。单质Y和W都可与浓的NaOH溶液反应。请回答下列问题:
(1)Y、Z、W的原子半径由小到大的顺序是________。
(2)ZW2的电子式是_________ 。
(3)X与Y化学性质相似,则X与浓的NaOH溶液反应的化学方程式是:_________ 。
【答案】
(1)
Cl<S<Al (2) 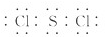 (3)
Be+2NaOH = Na2BeO2 + H2↑
(3)
Be+2NaOH = Na2BeO2 + H2↑
【解析】根据元素的结构及性质可知,X、Y、Z、W分别是Be、Al、S、Cl。
(1)同周期自左向右原子半径逐渐减小,所以原子半径大小顺序是Cl<S<Al。
(2)SCl2是含有极性键的共价化合物,电子式为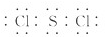 。
。
(3)应用Be和铝的性质相似,所以Be和氢氧化钠反应的方程式为Be+2NaOH = Na2BeO2 + H2↑。

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目

