题目内容
有甲、乙、丙三种溶液,进行如下操作:

则甲、乙、丙三种溶液可能是( )
A.BaCl2、H2SO4、MgCl2 B.CaCl2、HNO3、AgNO3
C.CaCl2、HNO3、NaCl D.BaCl2、HCl、NaNO3
练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案
相关题目
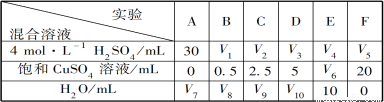
为研究硫酸铜的量对锌与稀硫酸反应氢气生成速率的影响,该同学设计了如下一系列实验。表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需的时间。下列说法正确的是
实验 混合溶液 | A | B | C | D | E | F |
4mol/LH2SO4溶液 | 30 | V1 | V2 | V3 | V4 | V5 |
饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
A. V1=30,V6=10
B.反应一段时间后,实验A,E中的金属呈暗红色
C.加入MgSO4与Ag2SO4可以起与硫酸铜相同的加速作用
D.硫酸铜的量越多,产生氢气的速率肯定越快
读下列药品标签,有关分析不正确的是( )
选项 | A | B | C | D |
物品标签 | 氢氧化钠固体 | 药品:浓硝酸 | 碳酸氢钠NaHCO3 | 浓硫酸H2SO4密度1.84g·mL-1 |
分析 | 该药品应装在带橡胶塞的广口瓶中密封保存 | 该药品标签上标有 | 受热易分解 | 该药品标签上标有 |


 O2(g)=H2O(g) ΔH1=a kJ·mol-1
O2(g)=H2O(g) ΔH1=a kJ·mol-1