题目内容
下列叙述错误的是( )
| A、氯水保存在棕色试剂瓶中 |
| B、Na2O2可用于呼吸面具中作为氧气的来源 |
| C、SiO2用于制造太阳能电池 |
| D、Fe2O3常用于制造红色油漆和涂料 |
考点:氯气的化学性质,硅和二氧化硅,钠的重要化合物,铁的氧化物和氢氧化物
专题:元素及其化合物,化学应用
分析:A.氯水中的次氯酸见光易分解;
B.过氧化钠与二氧化碳反应生成氧气;
C.高纯硅是制造太阳能电池主要原料;
D.氧化铁是红色固体.
B.过氧化钠与二氧化碳反应生成氧气;
C.高纯硅是制造太阳能电池主要原料;
D.氧化铁是红色固体.
解答:
解:A.氯水中含有次氯酸,次氯酸具有不稳定性,见光易分解,所以氯水应保存在棕色试剂瓶中,故A正确;
B.过氧化钠与二氧化碳反应生成氧气,所以Na2O2可用于呼吸面具中作为氧气的来源,故B正确;
C.高纯硅是制造太阳能电池主要原料,故C错误;
D.Fe2O3为红色物质,则常用作红色油漆和涂料,故D正确;
故选:C.
B.过氧化钠与二氧化碳反应生成氧气,所以Na2O2可用于呼吸面具中作为氧气的来源,故B正确;
C.高纯硅是制造太阳能电池主要原料,故C错误;
D.Fe2O3为红色物质,则常用作红色油漆和涂料,故D正确;
故选:C.
点评:本题考查物质的性质和用途,明确物质的性质是解答的关键,注意性质决定物质的用途,把握化学与生活的联系,题目难度不大.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目
下列物质的溶液中所含离子种类最多的是( )
| A、H2S |
| B、Na3PO4 |
| C、NaHCO3 |
| D、AlCl3 |
下列离子方程式书写正确的是( )
| A、铁跟盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
| B、向氯化铝溶液中通入氨气至过量:4NH3+Al3++2H2O=AlO2-+4NH4+ |
| C、次氯酸钙溶液中通入过量的CO2:ClO-+H2O+CO2=HCO3-+HClO |
| D、碳酸钙与盐酸反应CO32-+2H+=CO2↑+H2O |
下列说法正确的是( )
| A、金属单质和酸反应一定放出氢气 |
| B、含金属元素的离子一定是阳离子 |
| C、金属阳离子被还原一定得到金属单质 |
| D、金属单质在化学反应中只作为还原剂失去电子 |
下列物质中不可能由一种元素组成的是( )
| A、单质 | B、氧化物 |
| C、化合物 | D、混合物 |
下列说法或关系中,不正确的是( )
| A、有机物的熔点低,受热易分解,都能燃烧;有机物都是非电解质,不易导电 |
| B、有机物的化学反应比较复杂,一般较慢,且常伴有副反应发生 |
| C、沸点:正戊烷>2一甲基丁烷>2,2一二甲基丙烷 |
| D、同物质的量的物质完全燃烧耗O2量:已烷>环已烷>苯=苯甲酸 |
将二氧化碳通入Ba(OH)2稀溶液中,能正确表示其导电能力变化的是( )
A、 |
B、 |
C、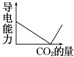 |
D、 |

 转变成
转变成 需经过哪几步合理的反应过程:
需经过哪几步合理的反应过程: